不整脈科
対象疾患・治療法
遺伝性不整脈疾患の遺伝子診断
遺伝性不整脈疾患の遺伝子診断
遺伝性不整脈疾患は、心筋の活動電位を形成するイオンチャネルとこれに関連する細胞膜蛋白、調節蛋白などをコードする遺伝子上の変異によりイオンチャネル機能障害をきたし、致死性不整脈を発症して心臓突然死の原因となる疾患です。遺伝性不整脈疾患には、先天性QT延長症候群(LQTS)、薬剤、電解質異常、徐脈などを原因とする後天性(二次性)LQTS、Brugada症候群、進行性心臓伝導欠損(PCCD, Lenegre病)、家族性徐脈症候群(洞機能不全症候群、房室ブロック)、カテコラミン誘発性多形性心室頻拍(CPVT)、QT短縮症候群(SQTS)などが含まれます。さらに最近では不整脈源性右室心筋症(ARVC/D)や徐脈を合併する拡張型心筋症(Laminopathy)なども特定の遺伝子異常が原因であることが分かってきています。
これらの遺伝性不整脈疾患の中でも遺伝子診断が最も進んでいるのは先天性LQTSです。先天性LQTSは現在15個の原因遺伝子が同定されていますが、そのほとんどがLQT1~3型であるため一般的な遺伝子検査ではLQT1~3型の遺伝子を調べます。その遺伝子診断率は50~70%であり、遺伝子診断結果が患者様の治療や生活指導に直接反映される(図1)ことから、平成20年より保険診療が適用されています(遺伝子診断料が8,000点(注1)、遺伝子カウンセリング料500点)。(注1) 2018年4月~(診療報酬点数改訂後)
国立循環器病研究センターの遺伝子検査室では、2001年6月から遺伝性不整脈疾患の遺伝子診断を開始しています。その数は年々増加し過去12年間に合計約3,700名の遺伝子検査を行ってきました(図2)。
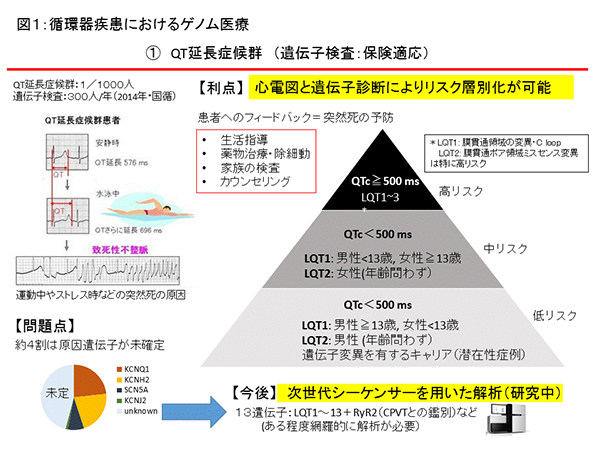
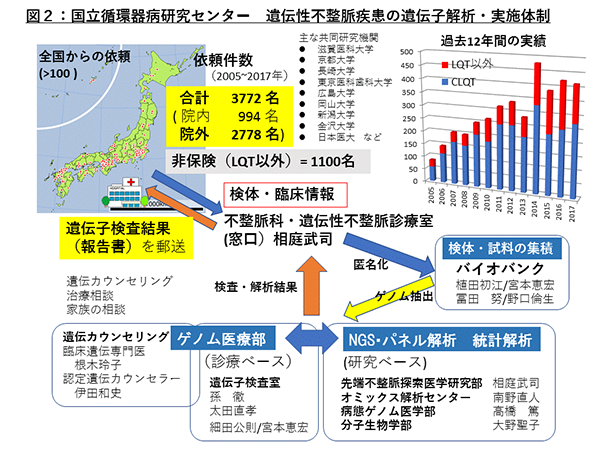
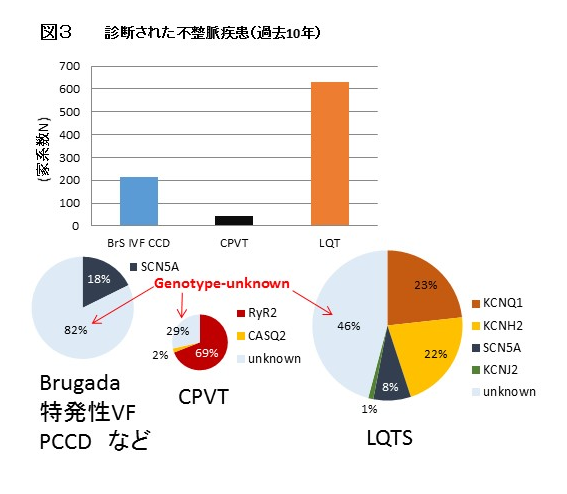
なかでも先天性LQTSは約2,600例(約1,300家系)に遺伝子検査を施行し、各遺伝子型の診断率は約60%でした。またBrugada症候群(PCCD/家族性徐脈含む)では約1,100例(約400家系)に遺伝子検査を施行し、その主な原因遺伝子のSCN5A診断率は約18%でした。CPVTでは100例(60家系)に遺伝子診断を施行し、遺伝子診断率は約70%でした(図3)。現在のところ不整脈疾患のなかで保険診療が認められているのは先天性LQTSだけですが、Brugada症候群とCPVTについては"診療目的での"遺伝子検査は自費診療にて行います(注2)。その他の遺伝性不整脈疾患(後天性LQTS、SQTS、特発性VF、家族性徐脈、家族性心房細動、ARVC、ラミノパチーなど)の遺伝子診断については、国立循環器病研究センターの研究費でさせていただいています。また未知の遺伝子異常の探索については、研究所と共同で次世代シーケンサー(NGS)を用いたパネル解析等により研究を行っています。
(注2) 2018年5月~実施予定(予定:45,500円)ただし発端者以外の家族スクリーニング分、研究が主目的の場合などでは従来どおり研究費負担で行う場合がありますので個別にご相談ください。
国立循環器病研究センターでは他院の患者様の遺伝子診断も積極的にお受けしています(図2)。遠方の場合当センターを受診していただかなくても、当センターと紹介元の診療機関の事務担当者間で事前に手続き(遺伝子診断料だけを保険または自費診療分を請求させて頂きます)をしていただければ、検査は可能です。遺伝子診断をご希望の場合には、まず事前にその適応があるか診療情報提供書をお送りください(国立循環器病研究センター専門医療連携室宛:FAX 06-6833-5126)。
関連プロジェクト(多施設共同研究を含む)(最近5年間)
| 2011年~ (現在) |
M21-031-7 遺伝性不整脈疾患の病因解明のための遺伝子解析と日本国内多施設登録 (研究責任者:相庭武司) |
| 2011年~ (現在) |
M21-030-3 難治性不整脈患者からのiPS細胞の樹立とそれを用いた疾患解析に関する研究 (研究責任者:相庭武司) |
| 2011年~ (現在) |
M22-031-5 特発性心室細動(Brugada症候群、早期再分極症候群)の病態と予後に関する多施設調査研究 (研究責任者:鎌倉 令) |
| 2018年~ | M25-132 アジア太平洋地域におけるブルガダ症候群患者の予後に関する臨床調査研究:Asia-Pacific Brugada syndrome Hereditary Registry Study (APHRS) (研究責任者:相庭武司) |
| 2018年~ | M22-048 遺伝性不整脈疾患の病因解明のための遺伝子解析ならびに多施設登録研究 [遺伝性不整脈登録研究] |
- 平成25-26年度文科省新学術領域研究
「統合的多階層生体機能学領域の確立とその応用」A02公募研究
『QT延長症候群における遺伝子変異部位別チャネル機能異常と不整脈基盤・予後との関係』
(代表研究者:相庭武司) - 平成27-29年度文科省科学研究費補助金 基盤研究C
「遺伝性不整脈疾患における突然死リスクの新しい非侵襲的評価法の開発」
(研究代表者:相庭武司) - 2015年度AMEDオーダーメイド医療の実現プログラム
「心臓突然死の発症リスク遺伝子の解明と層別化システムの構築」
(研究代表者:蒔田直昌(長崎大学)) - 平成28年度厚生労働科学研究費(難治性疾患政策研究事業)
「遺伝子診断に基づく不整脈疾患群の病態解明および診断基準・重症度分類・ガイドライン作成に関する研究」
(研究代表者:堀江稔(滋賀医科大学)) - 2016年度(平成28年度)AMED循環器疾患・糖尿病等生活習慣病対策実用化研究事業
「特発性心室細動の網羅的な遺伝子解析による突然死リスクと病態解明に関する研究」
(研究代表者:相庭武司) - 2017年度AMED難治性疾患実用化研究事業
「ブルガダ症候群における心臓突然死のリスク予測モデルの構築と診療応用のための研究」
(研究代表者:中野由紀子(広島大学)) - 2017年度日本循環器学会 循環器病におけるゲノム解析プロジェクト研究助成:
遺伝性不整脈疾患
(研究代表者:相庭武司) - 平成30年度 ゲノム医療実現推進プラットフォーム事業(先端ゲノム研究開発)
「マルチオミックス連関による循環器疾患における次世代型精密医療の実現」
(研究代表者:小室一成(東京大学))
関連論文業績(最近5年間)
- Inoue YY†, Aiba T†, Kawata H, Sakaguchi T, Mitsuma W, Morita H, Noda T, Takaki H, Toyohara K, Kanaya Y, Itoi T, Mitsuhashi T, Sumitomo N, Cho Y, Yasuda S, Kamakura S, Kusano K, Miyamoto Y, Horie M, Shimizu W. Different responses to exercise between Andersen-Tawil syndrome and catecholaminergic polymorphic ventricular tachycardia Europace (2017) in press doi:10.1093/europace/eux351.†: equal contribution.
- Milman A, Andorin A, Gourraud JB, Sacher F, Mabo P, Kim SH, Maeda S, Takahashi Y, Kamakura T, Aiba T, Conte G, Juang JJM, Leshem E, Rahkovich M, Hochstadt A, Mizusawa Y, Postema PG, Arbelo E, Huang Z, Denjoy I, Giustetto C, Wijeyeratne YD, Napolitano C, Michowitz Y, Brugada R, Casado-Arroyo R, Champagne J, Calo L, Sarquella-Brugada G, Tfelt-Hansen J, Priori SG, Takagi M, Veltmann C, Delise P, Corrado D, Behr ER, Gaita F, Yan GX, Brugada J, Leenhardt A, Wilde AAM, Brugada P, Kusano KF, Hirao K, Nam GB, Probst V, Belhassen B. Age of First Arrhythmic Event in Brugada Syndrome: Data From the SABRUS (Survey on Arrhythmic Events in Brugada Syndrome) in 678 Patients. Circ Arrhythm Electrophysiol.10(12), Dec 2017. pii: e005222. doi: 10.1161/CIRCEP.117.005222. Epub 2017 Dec 18.
- Kamakura T, Wada M, Ishibashi K, Inoue YY, Miyamoto K, Okamura H, Nagase S, Noda T, Aiba T, Yasuda S, Shimizu W, Kamakura S, Kusano K. Feasibility evaluation of long-term use of beta-blockers and calcium antagonists in patients with Brugada syndrome. Europace. 2017. doi: 10.1093/europace/eux198.
- Kashiwa A, Aiba T. Acquired Long-QT Syndrome: Mild but Abnormal? Intern Med. 8, Dec 2017. doi: 10.2169/internalmedicine.9731-17.
- Yamagata K, Aiba T, Shimizu W. Response by Yamagata et al to Letter Regarding Article, Genotype-Phenotype Correlation of SCN5A Mutation for the Clinical and Electrocardiographic Characteristics of Probands With Brugada Syndrome: A Japanese Multicenter Registry. Circulation. 5;136(23):2289-2290, Dec 2017.
- Aiba T, Takahashi A. QT interval determinant: Mutations, Rare variants, or Single-nucleotide Polymorphisms? Circ Cardiovasc Genet.10:e001945, 2017. DOI:10.1161/CIRCGENETICS.117.001945.
- Nishiuchi S, Makiyama T, Aiba T, Nakajima K, Hirose S, Kohjitani F, Yamamoto Y, Harita T, Hayano M, Wuriyanghai Y, Chen J, Sasaki K, Yagihara N, Ishikawa T, Onoue K, Murakoshi N, Watanabe I, Ohkubo K, Watanabe H, Ohno S, Doi T, Shizuta S, Minamino T, Saito Y, Oginosawa Y, Nogami A, Aonuma K, Kusano K, Makita N, Shimizu W, Horie M, Kimura T. Gene-1 based Risk Stratification for Cardiac Disorders in LMNA Mutation Carriers. Circ Cardiovasc Genet.10(6). pii: e001603, Dec 2017. doi: 10.1161/CIRCGENETICS.116.001603.
- Kitajima R, Aiba T, Kamakura T, Ishibashi K, Wada M, Inoue Y, Miyamoto K, Okamura H, Noda T, Nagase S, Kataoka Y, Asaumi Y, Noguchi T, Yasuda S, Kusano K. Landiolol suppression of electrical storm of torsades de pointes in patients with congenital long-QT syndrome type 2 and myocardial ischemia. J Arrhythm. 33(5):501-504. 2017
- Wada Y, Ohno S, Aiba T, Horie M. Unique genetic background and outcome of non-Caucasian Japanese probands with arrhythmogenic right ventricular dysplasia/cardiomyopathy. Molecular Genetics and Genomic Medicine,5(6):639-651, 2017.
- Kuroda Y, Yuasa S, Watanabe Y, Ito S, Egashira T, Seki T, Hattori T, Ohno S, Kodaira M, Suzuki T, Hashimoto H, Okata S, Tanaka A, Aizawa Y, Murata M, Aiba T, Makita N, Furukawa T, Shimizu W, Kodama I, Ogawa S, Kokubun N, Horigome H, Horie M, Kamiya K, Fukuda K. Flecainide ameliorates arrhythmogenicity through NCX flux in Andersen-Tawil syndrome-iPS cell-derived cardiomyocytes. Biochem Biophys Rep. 9:245-256, 2017. doi: 10.1016/j.bbrep.2017.01.002. eCollection 2017 Mar.
- Kimura Y, Takaki H, Inoue YY, Oguchi Y, Nagayama T, Nakashima T, Kawakami S, Nagase S, Noda T, Aiba T, Shimizu W, Kamakura S, Sugimachi M, Yasuda S, Shimokawa H, Kusano K. Isolated Late Activation Detected by Magnetocardiography Predicts Future Lethal Ventricular Arrhythmic Events in Patients With Arrhythmogenic Right Ventricular Cardiomyopathy. Circ J. 30, Aug 2017. doi: 10.1253/circj.CJ-17-0023.
- Kamakura T, Wada M, Ishibashi K, Inoue YY, Miyamoto K, Okamura H, Nagase S, Noda T, Aiba T, Yasuda S, Kusano K. Impact of electrocardiogram screening during drug challenge test for the prediction of T-wave oversensing by a subcutaneous implantable cardioverter defibrillator in patients with Brugada syndrome. Heart Vessels. 18, May 2017. doi: 10.1007/s00380-017-0994-3.
- Miyake A, Sakaguchi H, Miyazaki A, Miyoshi T, Aiba T, Shiraishi I. Successful prenatal management of ventricular tachycardia and second-degree atrioventricular block in fetal long QT syndrome. HeartRhythm Case Rep. 21;3(1):53-57, 2016.
- Kimura Y, Aiba T, Sasano T, Furukawa T, Kusano K, Shimizu W. IRX3 variant as a modifier of Brugada syndrome with frequent ventricular fibrillation. HeartRhythm Case Rep. 2(6):465-468, 2016.
- Kimura Y, Noda T, Matsuyama TA, Otsuka Y, Kamakura T, Wada M, Ishibashi K, Inoue Y, Miyamoto K, Okamura H, Nagase S, Aiba T, Kamakura S, Noguchi T, Anzai T, Satomi K, Wada Y, Ohno S, Horie M, Shimizu W, Yasuda S, Shimokawa H, Kusano K. Heart failure in patients with arrhythmogenic right ventricular cardiomyopathy: What are the risk factors? Int J Cardiol. 241:288-294, 2017.
- Yamagata K, Horie M, Aiba T, Ogawa S, Aizawa Y, Ohe T, Yamagishi M, Makita N, Sakurada H, Tanaka T, Shimizu A, Hagiwara N, Kishi R, Nakano Y, Takagi M, Makiyama T, Ohno S, Fukuda K, Watanabe H, Morita H, Hayashi K, Kusano K, Kamakura S, Yasuda S, Ogawa H, Miyamoto Y, Kapplinger JD, Ackerman MJ, Shimizu W. Genotype-Phenotype Correlation of SCN5A Mutation for the Clinical and Electrocardiographic Characteristics of Probands with Brugada Syndrome: A Japanese Multicenter Registry. Circulation. 135(23):2255-2270.2017
- Ishibashi K, Aiba T, Kamiya C, Miyazaki A, Sakaguchi H, Wada M, Nakajima I, Miyamoto K, Okamura H, Noda T, Yamauchi T, Itoh H, Ohno S, Motomura H, Ogawa Y, Goto H, Minami T, Yagihara N, Watanabe H, Hasegawa K, Terasawa A, Mikami H, Ogino K, Nakano Y, Imashiro S, Fukushima Y, Tsuzuki Y, Asakura K, Yoshimatsu J, Shiraishi I, Kamakura S, Miyamoto Y, Yasuda S, Akasaka T, Horie M, Shimizu W, Kusano K. Arrhythmia risk and β-blocker therapy in pregnant women with long QT syndrome. Heart. 14, Mar 2017. pii: heartjnl-2016-310617.
- Miyazaki A, Sakaguchi H, Matsumura Y, Hayama Y, Noritake K, Negishi J, Tsuda E, Miyamoto Y, Aiba T, Shimizu W, Kusano K, Shiraishi I, Ohuchi H. Mid-Term Follow-up of School-Aged Children With Borderline Long QT Interval. Circ J. 18, Feb 2017. doi: 10.1253/circj.CJ-16-0991.
- Ishikawa T, Ohno S, Murakami T, Yoshida K, Mishima H, Fukuoka T, Kimoto H, Sakamoto R, Ohkusa T, Aiba T, Nogami A, Sumitomo N, Shimizu W, Yoshiura KI, Horigome H, Horie M, Makita N. Sick sinus syndrome with HCN4 mutations shows early onset and frequent association with atrial fibrillation and left ventricular noncompaction. Heart Rhythm. 17, Jan 2017. pii: S1547-5271(17)30067-X. doi: 10.1016/j.hrthm.2017.01.020.
- Kamakura T, Wada M, Ishibashi K, Inoue YY, Miyamoto K, Okamura H, Nagase S, Noda T, Aiba T, Yasuda S, Shimizu W, Kamakura S, Kusano K. Differences in the onset mode of ventricular tachyarrhythmia between patients with J wave in anterior leads and those with J wave in inferolateral leads. Heart Rhythm. 23, Nov 2016. pii: S1547-5271(16)31074-8. doi: 10.1016/j.hrthm.2016.11.027.
- Mahati E, Li P, Kurata Y, Maharani N, Ikeda N, Sakata S, Ogura K, Miake J, Aiba T, Shimizu W, Nakasone N, Ninomiya H, Higaki K, Yamamoto K, Nakai A, Shirayoshi Y, Hisatome I. M3 Muscarinic Receptor Signaling Stabilizes a Novel Mutant Human Ether-a-Go-Go-Related Gene Channel Protein via Phosphorylation of Heat Shock Factor 1 in Transfected Cells. Circ J. 80(12):2443-2452, 2016.
- Ichikawa M, Aiba T, Ohno S, Shigemizu D, Ozawa J, Sonoda K, Fukuyama M, Itoh H, Miyamoto Y, Tsunoda T, Makiyama T, Tanaka T, Shimizu W, Horie M. Phenotypic Variability of ANK2 Mutations in Patients With Inherited Primary Arrhythmia Syndromes. Circ J. 80(12):2435-2442, 2016.
- Kondo T, Hisatome I, Yoshimura S, Mahati E, Notsu T, Li P, Iitsuka K, Kato M, Ogura K, Miake J, Aiba T, Shimizu W, Kurata Y, Sakata S, Nakasone N, Ninomiya H, Nakai A, Higaki K, Kawata Y, Shirayoshi Y, Yoshida A, Yamamoto K. Characterization of the novel mutant A78T-HERG from a long QT syndrome type 2 patient: Instability of the mutant protein and stabilization by heat shock factor 1. J Arrhythm. 32(5):433-440, 2016.
- Okata S, Yuasa S, Suzuki T, Ito S, Makita N, Yoshida T, Li M, Kurokawa J, Seki T, Egashira T, Aizawa Y, Kodaira M, Motoda C, Yozu G, Shimojima M, Hayashiji N, Hashimoto H, Kuroda Y, Tanaka A, Murata M, Aiba T, Shimizu W, Horie M, Kamiya K, Furukawa T, Fukuda K. Embryonic type Na+ channel β-subunit, SCN3B masks the disease phenotype of Brugada syndrome. Sci Rep. 28;6:34198, Sep 2016. doi: 10.1038/srep34198.
- Yagihara N, Watanabe H, Barnett P, Duboscq-Bidot L, Thomas AC, Yang P, Ohno S, Hasegawa K, Kuwano R, Chatel S, Redon R, Schott JJ, Probst V, Koopmann TT, Bezzina CR, Wilde AA, Nakano Y, Aiba T, Miyamoto Y, Kamakura S, Darbar D, Donahue BS, Shigemizu D, Tanaka T, Tsunoda T, Suda M, Sato A, Minamino T, Endo N, Shimizu W, Horie M, Roden DM, Makita N. Variants in the SCN5A Promoter Associated With Various Arrhythmia Phenotypes. J Am Heart Assoc. 13;5(9), Sep 2016. pii: e003644. doi: 10.1161/JAHA.116.003644.
- Wilde AA, Moss AJ, Kaufman ES, Shimizu W, Peterson DR, Benhorin J, Lopes C, Towbin JA, Spazzolini C, Crotti L, Zareba W, Goldenberg I, Kanters JK, Robinson JL, Qi M, Hofman N, Tester DJ, Bezzina CR, Alders M, Aiba T, Kamakura S, Miyamoto Y, Andrews ML, McNitt S, Polonsky B, Schwartz PJ, Ackerman MJ. Clinical Aspects of Type 3 Long-QT Syndrome: An International Multicenter Study. Circulation. 134(12):872-82, 2016.
- Ogawa Y, Aiba T, Kamei N, Tominaga K, Fujita H, Miyamoto Y, Tanaka T, Kido S. Coexistence of congenital long QT syndrome and autonomic dysregulation in children. Pediatr Int.58(7):672-4, 2016.
- Kawata H, Ohno S, Aiba T, Sakaguchi H, Miyazaki A, Sumitomo N, Kamakura T, Nakajima I, Inoue YY, Miyamoto K, Okamura H, Noda T, Kusano K, Kamakura S, Miyamoto Y, Shiraishi I, Horie M, Shimizu W. Catecholaminergic Polymorphic Ventricular Tachycardia (CPVT) Associated With Ryanodine Receptor (RyR2) Gene Mutations- Long-Term Prognosis After Initiation of Medical Treatment. Circ J. 80(9):1907-15, 2016.
- Taniguchi Y, Miyazaki A, Sakaguchi H, Hayama Y, Ebishima N, Negishi J, Noritake K, Miyamoto Y, Shimizu W, Aiba T, Ohuchi H. Prominent QTc prolongation in a patient with a rare variant in the cardiac ryanodine receptor gene. Heart Vessels. 32(2):229-233, 2017.
- Itoh H, Crotti L, Aiba T, Spazzolini C, Denjoy I, Fressart V, Hayashi K, Nakajima T, Ohno S, Makiyama T, Wu J, Hasegawa K, Mastantuono E, Dagradi F, Pedrazzini M, Yamagishi M, Berthet M, Murakami Y, Shimizu W, Guicheney P, Schwartz PJ, Horie M. The genetics underlying acquired long QT syndrome: impact for genetic screening. Eur Heart J. 2016 May 7;37(18):1456-64.
- Kamakura T, Wada M, Nakajima I, Ishibashi K, Miyamoto K, Okamura H, Noda T, Aiba T, Takaki H, Yasuda S, Ogawa H, Shimizu W, Makiyama T, Kimura T, Kamakura S, Kusano K. Significance of electrocardiogram recording in high intercostal spaces in patients with early repolarization syndrome. Eur Heart J. 2016 Feb 14;37(7):630-7.
- Funasako M, Aiba T, Ishibashi K, Nakajima I, Miyamoto K, Inoue Y, Okamura H, Noda T, Kamakura S, Anzai T, Noguchi T, Yasuda S, Miyamoto Y, Fukushima Kusano K, Ogawa H, Shimizu W. Pronounced Shortening of QT Interval With Mexiletine Infusion Test in Patients With Type 3 Congenital Long QT Syndrome. Circ J. 2016 Jan 25;80(2):340-5.
- Koizumi A, Sasano T, Kimura W, Miyamoto Y, Aiba T, Ishikawa T, Nogami A, Fukamizu S, Sakurada H, Takahashi Y, Nakamura H, Ishikura T, Koseki H, Arimura T, Kimura A, Hirao K, Isobe M, Shimizu W, Miura N, Furukawa T. Genetic defects in a His-Purkinje system transcription factor, IRX3, cause lethal cardiac arrhythmias. Eur Heart J. 2015 Oct 1 (in press).
- Shigemizu D, Aiba T, Nakagawa H, Ozaki K, Miya F, Satake W, Toda T, Miyamoto Y, Fujimoto A, Suzuki Y, Kubo M, Tsunoda T, Shimizu W, Tanaka T. Exome Analyses of Long QT Syndrome Reveal Candidate Pathogenic Mutations in Calmodulin-Interacting Genes. PLoS One. 2015 Jul 1;10(7):e0130329.
- Kamakura T, Wada M, Nakajima I, Ishibashi K, Miyamoto K, Okamura H, Noda T, Aiba T, Takaki H, Yasuda S, Ogawa H, Shimizu W, Makiyama T, Kimura T, Kamakura S, Kusano K. Evaluation of the necessity for cardioverter-defibrillator implantation in elderly patients with Brugada syndrome. Circulation Arrhythm Electrophysiol. 2015 Aug;8(4):785-91.
- Itoh H, Dochi K, Shimizu W, Denjoy I, Ohno S, Aiba T, Kimura H, Kato K, Fukuyama M, Hasagawa K, Schulze-Bahr E, Guicheney P, Horie M. A Common Mutation of Long QT Syndrome Type 1 in Japan. Circ J. 2015;79(9):2026-30.
- Wada Y, Aiba T, Matsuyama TA, Nakajima I, Ishibashi K, Miyamoto K, Yamada Y, Okamura H, Noda T, Satomi K, Morita Y, Kanzaki H, Kusano K, Anzai T, Kamakura S, Ishibashi-Ueda H, Shimizu W, Horie M, Yasuda S, Ogawa H. Clinical and Pathological Impact of Tissue Fibrosis on Lethal Arrhythmic Events in Hypertrophic Cardiomyopathy Patients With Impaired Systolic Function. Circ J. 2015;79(8):1733-41.
- Miyamoto K, Aiba T, Kimura H, Hayashi H, Ohno S, Yasuoka C, Tanioka Y, Tsuchiya T, Yoshida Y, Hayashi H, Tsuboi I, Nakajima I, Ishibashi K, Okamura H, Noda T, Ishihara M, Anzai T, Yasuda S, Miyamoto Y, Kamakura S, Kusano K, Ogawa H, Horie M, Shimizu W. Efficacy and safety of flecainide for ventricular arrhythmias in patients with Andersen-Tawil syndrome with KCNJ2 mutations. Heart Rhythm. 2015 Mar;12(3):596-603.
- Aiba T, Noda T, Hidaka I, Inagaki M, Katare RG, Ando M, Sunagawa K, Sato T, Sugimachi M. Acetylcholine Suppresses Ventricular Arrhythmias and Improves Conduction and Connexin-43 Properties During Myocardial Ischemia in Isolated Rabbit Hearts. J Cardiovasc Electrophysiol. 2015 Jun;26(6):678-85.
- Okamura H, Kamakura T, Morita H, Tokioka K, Nakajima I, Wada M, Ishibashi K, Miyamoto K, Noda T, Aiba T, Nishii N, Nagase S, Shimizu W, Yasuda S, Ogawa H, Kamakura S, Ito H, Ohe T, Kusano KF. Risk stratification in patients with Brugada syndrome without previous cardiac arrest - prognostic value of combined risk factors. Circ J. 2015;79(2):310-7.
- Arakawa J, Hamabe A, Aiba T, Nagai T, Yoshida M, Touya T, Ishigami N, Hisadome H, Katsushika S, Tabata H, Miyamoto Y, Shimizu W. A novel cardiac ryanodine receptor gene (RyR2) mutation in an athlete with aborted sudden cardiac death: a case of adult-onset catecholaminergic polymorphic ventricular tachycardia. Heart Vessels. 2015 Nov;30(6):835-40.
- Feng N, Huke S, Zhu G, Tocchetti CG, Shi S, Aiba T, Kaludercic N, Hoover DB, Beck SE, Mankowski JL, Tomaselli GF, Bers DM, Kass DA, Paolocci N. Constitutive BDNF/TrkB signaling is required for normal cardiac contraction and relaxation. Proc Natl Acad Sci U S A. 2015 Feb 10;112(6):1880-5.
- Makita N, Yagihara N, Crotti L, Johnson CN, Beckmann BM, Roh MS, Shigemizu D, Lichtner P, Ishikawa T, Aiba T, Homfray T, Behr ER, Klug D, Denjoy I, Mastantuono E, Theisen D, Tsunoda T, Satake W, Toda T, Nakagawa H, Tsuji Y, Tsuchiya T, Yamamoto H, Miyamoto Y, Endo N, Kimura A, Ozaki K, Motomura H, Suda K, Tanaka T, Schwartz PJ, Meitinger T, Kaab S, Guicheney P, Shimizu W, Bhuiyan ZA, Watanabe H, Chazin WJ, George AL. Novel Calmodulin (CALM2) Mutations Associated with Congenital Arrhythmia Susceptibility. Circulation Cardiovasc Genet. 2014 7(4); 466-74.
- Aiba T, Farinelli F, Kostecki G, Hesketh GG, Edwards D, Biswas S, Tung L, Tomaselli GF. A mutation causing Brugada syndrome identifies a mechanism for altered autonomic and oxidant regulation of cardiac sodium currents. Circulation Cardiovasc Genet. 2014 Jun;7(3):249-56.
- Kokunai Y, Nakata T, Furuta M, Sakata S, Kimura H, Aiba T, Yoshinaga M, Osaki Y, Nakamori M, Itoh H, Sato T, Kubota T, Kadota K, Shindo K, Mochizuki H, Shimizu W, Horie M, Okamura Y, Ohno K, Takahashi MP. A Kir3.4 mutation causes Andersen-Tawil syndrome by an inhibitory effect on Kir2.1. Neurology. 2014 Mar 25;82(12):1058-64.
- Bando S, Soeki T, Matsuura T, Niki T, Ise T, Yamaguchi K, Taketani Y, Iwase T, Yamada H, Wakatsuki T, Akaike M, Aiba T, Shimizu W, Sata M. Congenital long QT syndrome with compound mutations in the KCNH2 gene. Heart Vessels. 2014 Jul;29(4):554-9.
- Lichter JG, Carruth E, Mitchell C, Barth AS, Aiba T, Kass DA, Tomaselli GF, Bridge JH, Sachse FB. Remodeling of the sarcomeric cytoskeleton in cardiac ventricular myocytes during heart failure and after cardiac resynchronization therapy. J Mol Cell Cardiol. 2014 Jul;72:186-95.
- Bezzina CR, Barc J, Mizusawa Y, Remme CA, Gourraud JB, Simonet F, Verkerk AO, Schwartz PJ, Crotti L, Dagradi F, Guicheney P, Fressart V, Leenhardt A, Antzelevitch C, Bartkowiak S, Borggrefe M, Schimpf R, Schulze-Bahr E, Zumhagen S, Behr ER, Bastiaenen R, Tfelt-Hansen J, Olesen MS, Kaab S, Beckmann BM, Weeke P, Watanabe H, Endo N, Minamino T, Horie M, Ohno S, Hasegawa K, Makita N, Nogami A, Shimizu W, Aiba T, Froguel P, Balkau B, Lantieri O, Torchio M, Wiese C, Weber D, Wolswinkel R, Coronel R, Boukens BJ, Bezieau S, Charpentier E, Chatel S, Despres A, Gros F, Kyndt F, Lecointe S, Lindenbaum P, Portero V, Violleau J, Gessler M, Tan HL, Roden DM, Christoffels VM, Le Marec H, Wilde AA, Probst V, Schott JJ, Dina C, Redon R. Common variants at SCN5A-SCN10A and HEY2 are associated with Brugada syndrome, a rare disease with high risk of sudden cardiac death. Nature Genetics. 2013 Sep;45(9):1044-9.
- Aiba T, Barth AS, Hesketh GG, Hashambhoy YL, Chakir K, Tunin RS, Greenstein JL, Winslow RL, Kass DA, Tomaselli GF. Cardiac resynchronization therapy improves altered Na channel gating in canine model of dyssynchronous heart failure. Circulation Arrhythmia Electrophysiol. 2013 Jun;6(3):546-54.
- Kamakura T, Kawata H, Nakajima I, Yamada Y, Miyamoto K, Okamura H, Noda T, Satomi K, Aiba T, Takaki H, Aihara N, Kamakura S, Kimura T, Shimizu W. Significance of non-type 1 anterior early repolarization in patients with inferolateral early repolarization syndrome. J Am Coll Cardiol. 2013 Oct 22;62(17):1610-8.
- Nakano Y, Chayama K, Ochi H, Toshishige M, Hayashida Y, Miki D, Hayes CN, Suzuki H, Tokuyama T, Oda N, Suenari K, Uchimura-Makita Y, Kajihara K, Sairaku A, Motoda C, Fujiwara M, Watanabe Y, Yoshida Y, Ohkubo K, Watanabe I, Nogami A, Hasegawa K, Watanabe H, Endo N, Aiba T, Shimizu W, Ohno S, Horie M, Arihiro K, Tashiro S, Makita N, Kihara Y. A nonsynonymous polymorphism in semaphorin 3A as a risk factor for human unexplained cardiac arrest with documented ventricular fibrillation. PLoS Genet. 2013 Apr;9(4):e1003364.
- Kawata H, Morita H, Yamada Y, Noda T, Satomi K, Aiba T, Isobe M, Nagase S, Nakamura K, Fukushima Kusano K, Ito H, Kamakura S, Shimizu W. Prognostic significance of early repolarization in inferolateral leads in Brugada patients with documented ventricular fibrillation: a novel risk factor for Brugada syndrome with ventricular fibrillation. Heart Rhythm. 2013 Aug;10(8):1161-8.
- Kawakami H, Aiba T, Yamada T, Okayama H, Kazatani Y, Konishi K, Nakajima I, Miyamoto K, Yamada Y, Okamura H, Noda T, Satomi K, Kamakura S, Makita N, Shimizu W. Variable phenotype expression with a frameshift mutation of the cardiac sodium channel gene SCN5A. Journal of Arrhythmia 2013; 29(5):291-295.
最終更新日:2021年10月08日
