広報活動
新しい抗凝固薬milvexianの脳梗塞患者を対象とした開発:第二相国際無作為化比較試験AXIOMATIC-SSPから 第三相Librexia STROKEへ
2023年12月14日
国立研究開発法人国立循環器病研究センター
国立循環器病研究センター(大阪府吹田市、理事長:大津欣也、略称:国循)の豊田一則副院長が国内調整医師を務めた、脳梗塞患者を対象とする国際第二相無作為化比較試験AXIOMATIC-SSPの試験成績が、2023年12月13日に医学雑誌「Lancet Neurology」オンライン版に掲載されました。
【背景】
脳梗塞や心臓血管病に多くの抗血栓薬(抗凝固薬と抗血小板薬)が臨床応用されていますが、これらの薬剤に共通する副作用に出血合併症があります。内因系凝固因子の凝固第XI因子は、凝固反応の増幅期に関わり血栓の成長および安定化に寄与しますが、止血に必須ではありません。先天性凝固第XI因子欠乏症患者では自然出血は稀で、凝固第XI因子欠乏患者では静脈血栓症、脳梗塞が比較的少ないことも知られています。凝固第XI因子阻害は、止血機序には影響せずに病的血栓形成を抑制する可能性があります。
Milvexian(BMS-986177/JNJ-70033093)は活性化凝固第XI因子を直接阻害する経口薬です。本剤を膝関節置換術後に用いることで、低分子ヘパリンであるエノキサパリンと比べて静脈血栓塞栓症の発現を抑止することが、無作為化試験で証明されています。Milvexianが脳梗塞患者に対しても再発予防効果を示すかを、国際試験で検討しました。
【研究方法】
Antithrombotic treatment with FXIa inhibition to Optimize Management of Acute Thromboembolic events for Secondary Stroke Prevention (AXIOMATIC-SSP)試験は、第二相、国際、多施設共同、無作為化、二重盲検、偽薬対照、用量設定試験です(ClinicalTrials.gov, NCT03766581)。発症後48時間以内の非心原性脳梗塞(非ラクナ性、重症度を示すNIH脳卒中尺度が7以下)ないし一過性脳虚血発作(脳卒中発症リスクを示すABCD2スコアが6以上または運動症状あり)の患者を対象としました。全例に21日後までクロピドグレルとアスピリンの抗血小板薬二剤併用を、その後90日後までアスピリンのみを処方したうえで、milvexian 5用量(1回量25mgを1日1回、または1回量25mg, 50mg, 100mg, 200mgを1日2回)ないし偽薬のいずれかを、90日後まで処方しました。有効性主要評価項目は90日以内の症候性脳梗塞(神経症候の出現を伴う脳梗塞)発症または90日後MRIでの無症候性脳梗塞(画像診断で梗塞巣を認めるものの神経症候を伴わない脳梗塞)出現で、これと別に症候性脳梗塞発症のみの結果も調べました。安全性主要評価項目は90日以内のBleeding Academic Research Consortium(BARC)基準でタイプ3とタイプ5に当たる大出血でした。
【結果】
2019年1月から2021年12月までに、世界全体で2366例(平均年齢69.6歳、女性36%)が登録され、日本から世界第2位の患者数の登録が行われました。有効性主要評価項目では、milvexianの有意な用量反応性を認めず、いずれの群も偽薬群と同等の発現率を呈しました(図1A)。脳梗塞発症に評価項目を絞った場合、いずれの群も偽薬群と有意差は認めないものの、200mg・1日2回群を除く全てのmilvexian群で、偽薬群よりも2~3割程度低い発症率を示しました(図1B)。安全性主要評価項目に関しても、いずれのmilvexian群も偽薬群と有意差を認めず、25mg・1日1回群と25mg・1日2回群での発症率は偽薬群と同程度でした(図1C)。BARCタイプ3cに当たる症候性頭蓋内出血は併せて6例(偽薬2/682例、25mg・1日2回 3/325例、200mg・1日2回 1/344例)に認めたのみで、BARCタイプ5の致死的出血は、1例も認めませんでした。
【解説】
非心原性脳梗塞の急性期から発症90日後にかけて既存の抗血小板薬にmilvexianを併用することによって、症候性脳梗塞および無症候性脳梗塞を併せた発現率は、milvexian各用量群での用量反応性が見られませんでしたが、症候性脳梗塞発症率に関しては、有意差はないものの多くのmilvexian群で偽薬(+抗血小板薬)群より低率でした。大出血についてはmilvexian各群、偽薬群とも1~2%の低い発症率でした。
本試験の結果を受けて脳梗塞・一過性脳虚血発作患者に対する脳卒中再発抑制を目的としたmilvexianの有効性と安全性を検討する第3相無作為化比較試験Librexia STROKEが、2023年より日本を含めた世界47か国で開始されました。
【謝辞】
AXIOMATIC-SSP試験は、ブリストル・マイヤーズ スクイブとヤンセンファーマからの助成を受けて行われました。
【論文情報】
著者:Mukul Sharma(カナダMcMaster大学), Carlos A. Molina(スペインVall d´Hebron大学), Kazunori Toyoda(国循), Daniel Bereczki(ハンガリーSemmelweis大学), Shrikant I. Bangdiwala(カナダMcMaster大学), Scott E. Kasner(米国Pennsylvania大学), et al
論文名:Safety and efficacy of factor XIa Inhibition with milvexian for secondary stroke prevention (AXIOMATIC-SSP): an international, multicentre, randomised, double-blind, placebo controlled, dose-finding phase 2 trial
掲載雑誌:Lancet Neurology
| 図1. 有効性、安全性の群間比較 |
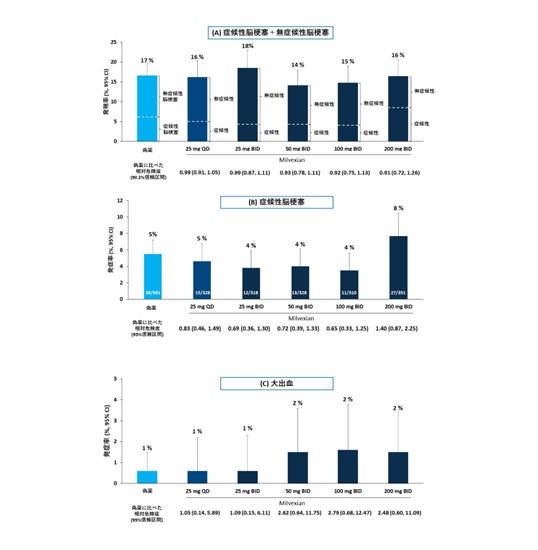 |
【報道機関からの問い合わせ先】
国立循環器病研究センター企画経営部広報企画室
TEL : 06-6170-1069(31120)
MAIL: kouhou@ml.ncvc.go.jp
最終更新日:2023年12月14日
