広報活動
人工心肺システム「BR13030」を用いた 急性重症心不全/急性重症呼吸不全患者に対する 補助循環法の安全性および有効性に関する 多施設共同単一群試験(NCVC-ECMO_01)
令和2年4月10日
国立循環器病研究センター
国立循環器病研究センター(大阪府吹田市、理事長:小川久雄、略称:国循)移植医療部の福嶌敎偉部長とオープンイノベーションセンターの巽英介副センター長らの研究チームは、小型・軽量で、長期間使用可能な次世代型人工心肺システム「BR13030(図1)」を世界に先駆けて開発しました。そしてこのたび、BR13030を用いた重症呼吸不全・心不全患者に対する補助循環(NCVC-ECMO _01)のfirst in human試験(初めて人体に医薬品や医療機器を投与してその有用性や安全性を確認する試験)を令和2年3月10日から医師主導治験として国循並びに、大阪大学医学部附属病院、関西医科大学総合医療センターの3施設で実施することとなりました。
背景
人工心肺システム(以下、ECMO)(注1)は人工呼吸器や昇圧剤使用など従来の治療法では救命困難な重症呼吸・循環不全の症例に用いられます。元々心臓外科手術に用いられる人工心肺装置から発展したECMOの臨床応用は、近年では救命救急領域や集中治療領域にまで広がりを見せ、その有用性は高まりつつあります。
主に循環のサポートを目的とするVA-ECMO(静脈脱血-動脈送血 ECMO)は、従来の薬物療法、外科的療法 、不整脈治療や機械的補助循環法では十分な効果が得られない重症心不全、心原性ショックの患者に対して適応があり、循環不全に呼吸不全が合併する場合にも応用できます。代表的な疾患には、各種心疾患(心筋症、二次性心筋症、虚血性心筋症、心筋炎)による低心拍出量症候群、急性心筋梗塞後心原性循環不全、体外循環離脱困難症などがあり、国内外のECMO使用例の90%はVA-ECMOです。
呼吸だけのサポートを目的とするVV-ECMO(静脈脱血-静脈送血 ECMO)は、可逆性急性呼吸不全に対する患者において適応があり、従来の人工呼吸管理では生命が維持できない場合、またはそれを続けることによって肺に不可逆的な傷害を与える可能性がある場合に使用を考慮します。代表的な疾患には、重症ウイルス性・細菌性肺炎、誤嚥性肺炎、急性呼吸窮迫症候群(Acute respiratory distress syndrome:ARDS)、肺移植へのブリッジ、移植肺機能不全(再灌流障害)、肺障害に起因する体外循環離脱困難症、喘息重積発作などがあります。現在、アウトブレイクしているCOVID-19や、これまでにアウトブレイクが報告されているSARS、MARS、H5N1鳥インフルエンザなどによる重症呼吸不全の有効な治療手段となることも期待されます。
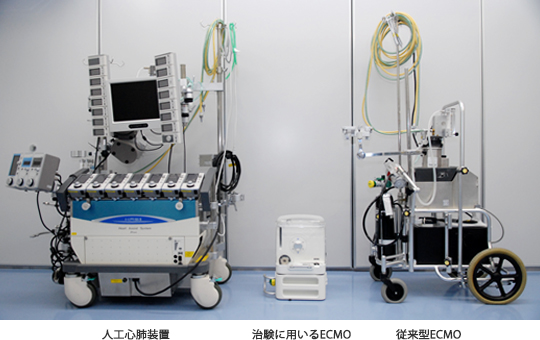
しかし、現在汎用されている装置は大きくて複雑なため(図2)緊急対応には不向きで、重症患者の救急搬送時など院外での使用も難しい状況です。また、抗血栓性や耐久性も不十分なため血栓塞栓症や出血合併症のリスクが高く、長期使用も困難です。現在、薬機法(注2)上承認されている使用期間は6時間以内に限られています。このため、院内・院外を問わず、装着が容易で安全に長期間使用可能なECMOシステムの開発が望まれていました。
機器概要と研究成果
国循人工臓器部では1986年より抗血栓性と長期耐久性に優れたECMOシステムの開発を目指して研究を続けてきました。本装置では、これまで人工臓器部が実用化してきた様々な先端技術を取り入れることで、高い緊急対応性・携帯性・抗血栓性・耐久性を実現しました。
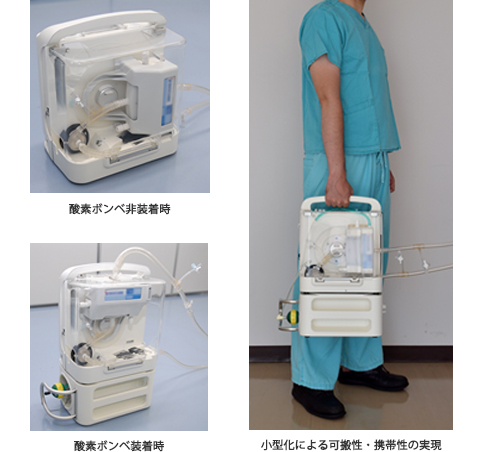
本装置は小型・軽量(29×20×26cm、6.6kg)で、簡単に持ち運びができます。(図1)緊急対応性を実現するために、専用回路ユニットを多機能集積型の超小型駆動装置に装填して即座に使用できるシステムとしており、4分以内の迅速な起動が可能です(易装着性)。また、電源や酸素供給のない場所でも、内臓バッテリと脱着型酸素ボンベユニットにより1時間の連続使用が可能です。このため、救急車での搬送中など院外の緊急装着にも対応できます。さらに、本装置には人工臓器部が過去に開発した優れた抗血栓技術が用いられており、抗凝固療法を最小限に抑えられます(安全性)。このため、血栓性および出血性合併症を防いで安全性を高めることができます。長期耐久性についても、本装置を用いた長期動物実験で装着後2週間(4例)および4週間(3例)の連続心肺補助を行いましたが、全例において予定期間を問題なく完遂することができました。
実施手法と今後の展望
本治験は、従来の治療法では救命が困難な重症呼吸不全・心不全の患者を対象に、最長14日間同じ回路で呼吸・循環補助を行うことで救命率の向上につながることの確認のために実施します。対象症例数はVA-ECMOとVV-ECMOの合計25 例(解析対象として23例)とし、うち、14日使用2例以上、VV-ECMO使用3例以上の実施を目標とし、症例登録期間は2020年2月10日~2022年3月31日(約2年間)とします。
本治験によりBR13030の効果が確認できれば、重篤な患者の救命に寄与する医療機器となることが期待されます。今後は早期の薬事承認を目指します。
謝辞
本研究は、主に下記機関より資金的支援を受け実施されました。
・日本医療研究開発機構(AMED) 医工連携事業化推進事業
「世界最小最軽量の高機能次世代型心肺補助システムの開発・事業化」(平成29~31年)
・日本学術振興会(JSPS) 科学研究費助成事業 基盤研究A
「救急~長期使用が可能な世界最小最軽量ヘパリンフリーECMOシステムの開発と製品化」(平成29~31年)
※その他、本ECMO装置の開発に関しては、複数機関より資金的支援を受けています。
<注釈>
(注1)ECMO
体外式膜型人工肺(Extracorporeal Membrane Oxygenation)の略称。人工肺とポンプを用いた体外循環回路による治療で、重症呼吸・循環不全患者の呼吸および循環回路が自発的に回復するまでの間に呼吸や循環を補助する対症療法として用いられる。経皮的心肺補助(Percutaneous Cardio Pulmonary Support:PCPS)も広義のECMOに含まれる。
(注2)薬機法
正確な名称は「医薬品・医療機器等の品質・有効性及び安全性の確保等に関する法律」。旧薬事法を平成25年に見直したもの。
<図>
(図1)今回の医師主導治験で用いられるECMO
(図2)従来機器との比較
最終更新日 2020年4月10日
最終更新日:2021年09月26日
