広報活動
アルテプラーゼによる血栓溶解療法はFLAIR検査で脳梗塞所見がでていない発症時刻が不明の脳梗塞患者に安全
令和2年3月30日
国立循環器病研究センター
日本医療研究開発機構
国立循環器病研究センター(大阪府吹田市、理事長:小川久雄、略称:国循)の豊田一則 副院長が研究代表者を務める国内多施設共同研究チームは、これまで発症時刻が不明の脳梗塞は静注血栓溶解療法の対象になり難かったのですが、頭部MRIの検査結果で発症から時間が経過していない所見であれば、静注血栓溶解療法を安全に行うことができることを無作為割付試験(注1)(THAWS試験(注2))により解明しました。今後は海外の同種試験と統合解析を行い、本治療法の有効性と安全性の更なる検討を行う予定です。本研究成果は国循古賀政利 脳血管内科部長らによって、Stroke誌電子版に令和2年4月6日付で発表されます。
背景
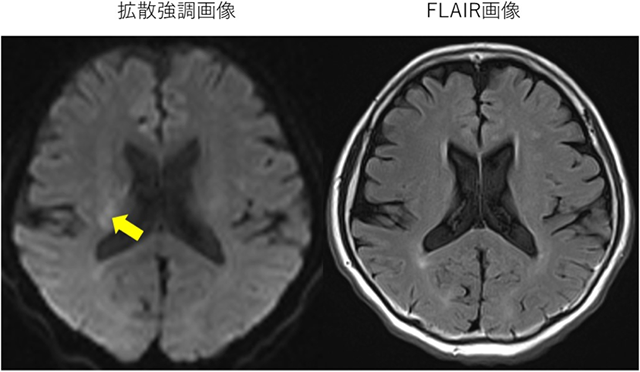
脳梗塞は死因の第4位、要介護疾患の上位を占める重要な国民病です。発症4.5時間以内の脳梗塞患者に対してはアルテプラーゼ静注による血栓溶解療法が有効ですが、発症時刻が不明の脳梗塞では最終健常確認時刻を発症時刻(最後に異常ではないと確認された時間)とみなすため、静注血栓溶解療法の適応になり難いことが問題でした。起床時に言葉の問題や手足の麻痺が判明する脳梗塞は発症時刻が不明の脳梗塞の代表であり、全脳梗塞の約2割を占めます。一方、頭部MRI検査を行い拡散強調画像(注3)上の脳梗塞所見がFLAIR画像(注4)で明らかではない場合(図1)は、発症から4.5時間以内である可能性が高いことが示されています。そこで、このFLAIR陰性所見を示す患者に対して、アルテプラーゼ静注による血栓溶解療法の有効性と安全性を調べました。
研究方法と成果
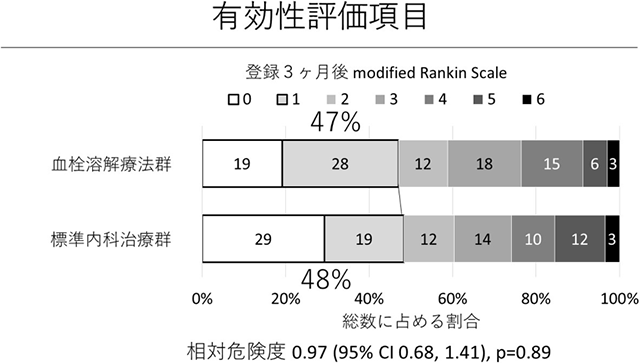
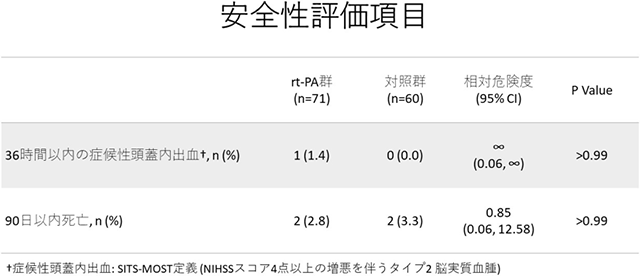
欧州で行われていたWAKE-UP試験と同様の結果を得ることを目標に、300例を登録する多施設無作為割付オープンラベル盲検下エンドポイント評価試験を行いました。発症時刻が不明の脳梗塞でFLAIR陰性所見を認める患者を、アルテプラーゼ0.6mg/kg静注療法群(71例)と標準内科治療群(対照群:60例)に無作為に割り付けて有効性と安全性を評価しました。WAKE-UP試験が先に終了して静注血栓溶解療法の有効性が証明されたことを受けて、131例(44%)を登録して試験を終了しました(表1)。有効性の指標では、登録3ヶ月後完全自立(modified Rankin Scale 0-1)の割合が静注療法群47%(32例/68例)と標準内科治療群(対照群)48%(28例/58例)(相対危険度0.97、95%信頼区間0.68-1.41、p=0.892)であり、2群間で統計的な有意差はありませんでした(図2)。安全性の指標では、治療開始後22-36時間後の症候性頭蓋内出血の割合が静注療法群と対照群では各1.4%(1例/71例)と0%(0例/60例)(p>0.999)、90日以内の死亡率が静注療法群と対照群で各々2.8%(2例/71例)と3.3%(2例/60例)(p>0.999)であり、2群間で統計的な有意差はありませんでした(表2)。
今後の展望と課題
試験期間中に脳主幹動脈閉塞(注5)による脳梗塞に対する血栓回収療法の有効性が確立したため、脳主幹動脈閉塞の患者の登録がほとんどなかったことが結果に影響した可能性があります。また、オープンラベル試験(注6)であったため結果的に標準内科治療群(対照群)に対して登録直後から積極的な抗血栓療法を行ったことが、この群における完全自立が多かった原因かもしれません。2019年3月に改訂された静注血栓溶解(rt-PA)療法の適正治療指針(第三版)では、FLAIR陰性所見を示す発症時刻が不明の脳梗塞の患者に対する静注血栓溶解療法を考慮してもよいことが示されましたので、有効性と安全性を検討する観察研究を行っています。更に、4つの同種試験(注7)との統合解析を行っており、発症時刻が不明の脳梗塞に対する静注血栓溶解療法の有効性と安全性の更なる検討を行い、本療法の確立に向けて研究を継続していきます。
謝辞
本研究は、下記機関より資金的支援を受け実施されました。
・AMED循環器疾患・糖尿病等生活習慣病対策実用化研究事業「発症時刻不明の急性期脳梗塞に対する適正な血栓溶解療法の推進を目指す研究」
<用語解説>
(注1)無作為割付試験:治療内容をランダムに割り当てて治療効果を調べる試験のこと。
(注2)THAWS試験:THrombolysis for Acute Wake-up and unclear-onset Strokes with alteplase at 0.6 mg/kg試験のこと。
(注3)拡散強調画像:核磁気共鳴画像法 (MRI) のシーケンスの一種であり、水分子の拡散運動を画像化したもの。
(注4)FLAIR画像:液体を減衰させた反転回復(IR)法の一種であり、反転時間 (TI) を脳脊髄液(CSF)の磁化がゼロ点を通る時間(大体2000ミリ秒)に設定し、CSF信号を抑制する撮像法で画像化したもの。
(注5)脳主幹動脈閉塞:脳に酸素や栄養を送っている複数の太い血管の主幹動脈が血栓や塞栓により突然閉塞を起こすこと。
(注6)オープンラベル試験:被験者にどの試験治療が割付けられたか医師、被験者、スタッフ全員に知られている試験のこと。
(注7)4つの同種試験:WAKE-UP試験(FLAIR陰性の発症時刻不明脳梗塞を対象としたアルテプラーゼ0.9mg/kgによる静注血栓溶解療法のプラセボ対象無作為割付二重盲検試験)、EXTEND試験(最終健常確認後4.5-9時間の脳梗塞を対象とし、脳灌流画像により症例選択したアルテプラーゼ0.9mg/kgによる静注血栓溶解療法のプラセボ対象無作為割付二重盲検試験)、ECASS-4試験(EXTEND試験と同様)、MR-WITNESS試験(FLAIR陰性の発症時刻不明脳梗塞を対象としたアルテプラーゼ0.9mg/kgによる静注血栓溶解療法の単一治療群試験)のことである。
<図>
(図1)FLAIR陰性所見
(表1) THAWS試験への患者登録施設
| 登録症例数 | 施設名 |
|---|---|
| 29例 | 国立循環器病研究センター |
| 13例 | 美原記念病院 |
| 11例 | 山形市立病院済生館 |
| 9例 | 帯広厚生病院 |
| 6例 | 広南病院、中村記念病院 |
| 5例 | 岐阜大学 |
| 4例 | 日本医科大学、秋田県立脳血管研究センター、佐賀大学 |
| 3例 | 新潟市民病院、京都第二赤十字病院、東海大学、九州医療センター、 岩手県立中央病院、長崎大学、トヨタ記念病院、大西脳神経外科病院 |
| 2例 | 川﨑医科大総合医療センター、徳島大学、聖マリアンナ医科大学、 製鉄記念八幡病院、杏林大学、神戸市立医療センター中央市民病院 |
| 1例 | 虎の門病院、兵庫医科大学、順天堂大学浦安病院、聖マリアンナ東横病院 |
(図2)有効性の指標
| modified Rankin Scale(mRS)の詳細は以下の通りです。 | |
| mRS 0 まったく症候がない | mRS 4 中等度から重度の障害 |
| mRS 1 症候はあっても明らかな障害はない | mRS 5 重度の障害 |
| mRS 2 軽度の障害 | mRS 6 死亡 |
| mRS 3 中等度の障害 | |
(表2)安全性の指標
最終更新日 2020年4月6日
最終更新日:2021年09月26日
