循環動態制御部
研究内容
心臓・血管力学の研究
心臓・血管力学の研究
私たちは、臨床において遭遇する多様な循環病態を定量的に説明することができるよう、循環器系の力学的モデル化を行いました。このモデルをもとに、急性心不全や敗血症性ショックなど重症で致命的な循環病態を評価し、さらに循環蘇生のための心血管作動薬治療をコンピュータ自動制御により最適化できる、画期的循環管理システムの開発を行ってきました。さらに、このようなシステムの臨床応用にも必要不可欠な、血圧・心拍出量や左心房圧の計測を低侵襲に行うための、画期的な循環モニタの開発も行っています。
(1) 循環器系全体のモデル化を用いた急性循環不全の血行動態自動治療システムの開発
私たちはガイトンの循環平衡理論を拡張し、多様な循環病態を取り扱うことができる循環平衡モデルを確立しました。このモデルは全循環系を左右心室とそれらの後負荷からなる心臓部、全身・肺循環からなる血管部に分離し、心拍出量・左心房圧・右心房圧の3次元座標上で解析します。心臓部からの心拍出量は、左右心房圧増加により増加し(フランクスターリング法則)、座標上では統合心拍出量曲線として表されます(図1)。血管部から心臓部への静脈還流量は左右心房圧が増加すれば減少し、座標上では両心房圧に対して負の傾きを持った静脈還流平面として表されます。
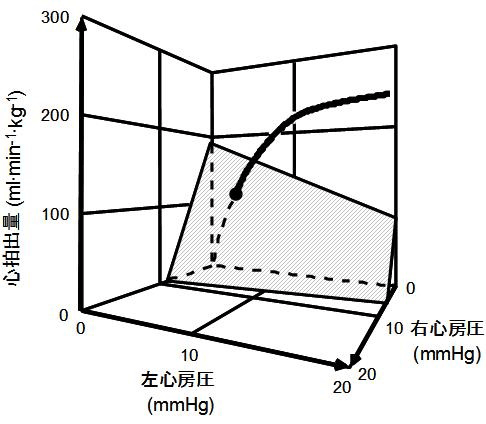
図1
関連成果等
- Uemura K, Sugimachi M, Kawada T, Kamiya A, Jin Y, Kashihara K, Sunagawa K. A Novel Framework of Circulatory Equilibrium. Am J Physiol Heart Circ Physiol 286: H2376-2385, 2004.
急性心不全や敗血症性ショックの患者救命には、複数の心血管作動薬を用いて異常な血圧・心拍出量・左心房圧を正常化する必要があります。私たちは、循環平衡モデルに基づき、心拍出量曲線、静脈還流平面、血管抵抗を個別に正常化させる負帰還制御により、血圧・心拍出量・左心房圧を同時に自動的に正常化できるシステムを開発しました。図2は、心不全犬での心血管作動薬投与システムの自動制御により、血圧・心拍出量・左心房圧は制御目標値からの誤差が速やかにかつ高い精度・安定性で収束し、血行動態を正確に制御できたことが示されています。図3は、敗血症性ショック犬で、循環蘇生を自動制御する際、心抑制のリスクがあるベータ遮断薬(ランジオロル)を投与しても蘇生は安定し、さらに心筋酸素代謝が改善し得たことを示しています。このように、私たちが開発してきた多様なシステムにより、循環器非専門医・集中治療非専門医にも高度な循環管理が可能となることが期待されます。
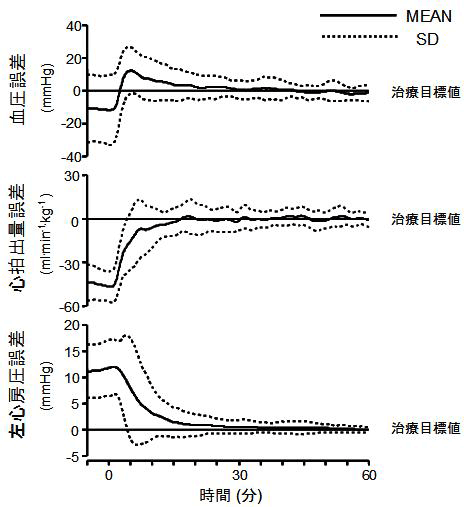
図2
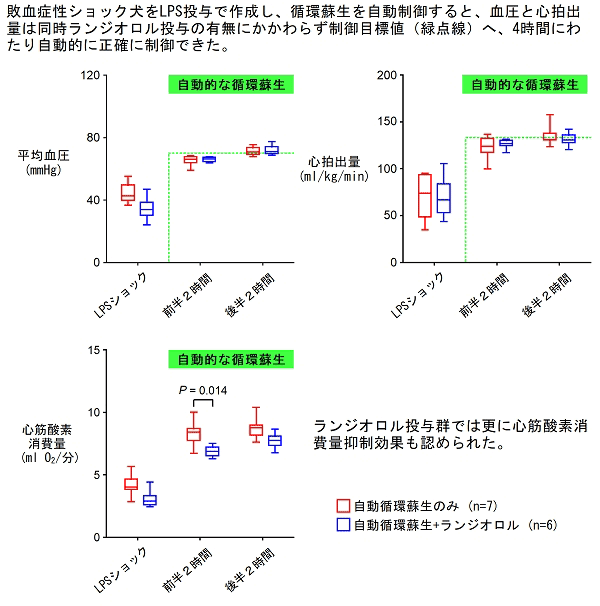
図3
関連成果等
- Uemura K, Kamiya A, Hidaka I, Kawada T, Shimizu S, Shishido T, Yoshizawa M, Sugimachi M, Sunagawa K. Automated drug delivery system to control systemic arterial pressure, cardiac output, and left heart filling pressure in acute decompensated heart failure. J Appl Physiol 100: 1278-1286, 2006.
- Uemura K, Kawada T, Zheng C, Li M, Sugimachi M. Computer-controlled closed-loop drug infusion system for automated hemodynamic resuscitation in endotoxin-induced shock. BMC Anesthesiol. 2017 Oct 23;17(1):145.
- Uemura K, Kawada T, Zheng C, Li M, Sugimachi M. Low-Dose Landiolol Reduces Heart Rate and Cardiac Oxygen Consumption Without Compromising Initial Hemodynamic Resuscitation in a Canine Model of Endotoxin Shock. Shock. 52: 102-110, 2019.
- 心疾患治療システム 特許登録 2006-544733(2004/11/18)
- 心疾患診断システム 特許登録 2006-544732(2004/11/18)
(2) 血行動態の低侵襲測定法の開発
循環病態を正確に把握するには血圧・心拍出量・左心房圧の3指標を正確に把握することが重要です。私たちは、これら3指標を低侵襲・低ストレスに正確かつ長期連続測定できる方法を開発してきました。
血圧は一般的に腕に巻いたカフを膨張させ、収縮期血圧以上にカフ圧を上げて計測します。しかしこのような計測は時として患者にとってストレスになり、特に血圧を24時間連続して計測する自由行動下血圧測定(ABPM)では大きな問題になってきます。この問題を解決するため、一般的なカフ式血圧計に薄型超音波プローブを組み込むことで、カフ圧上昇を低い範囲(<50 mmHg)に抑制しながら正確に血圧測定できるストレスフリーABPMを開発しました(図4)。
心拍出量・左心房圧測定は一般的に、肺動脈カテーテルにより侵襲的に計測されますが、合併症の多さや予後改善効果の欠如から、その使用が見直されてきています。この状況を克服するため、超音波ドップラーによる心拍出量・左心房圧の正確な低侵襲モニタ法を開発してきました。基礎的開発研究において、左心房圧は右心房圧(静脈圧)と、超音波心エコーで計測する左右の心ポンプ機能比から推定できることを明らかにし、このようにして開発した左心房圧推定法の臨床有用性を、病院心臓内科との共同研究で心不全症例において実証しました(図5)。さらにこれらの低侵襲測定法を用いた血行動態の自動治療が可能であることも実証しました。
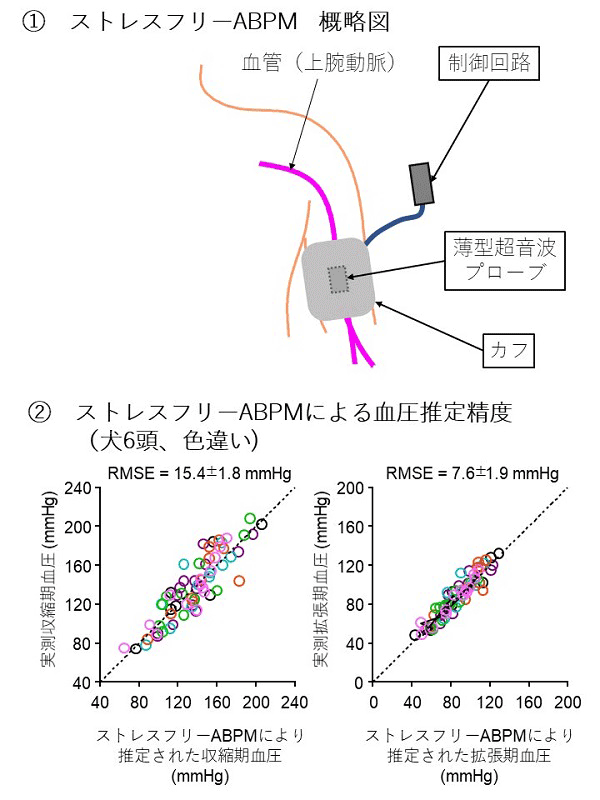
図4
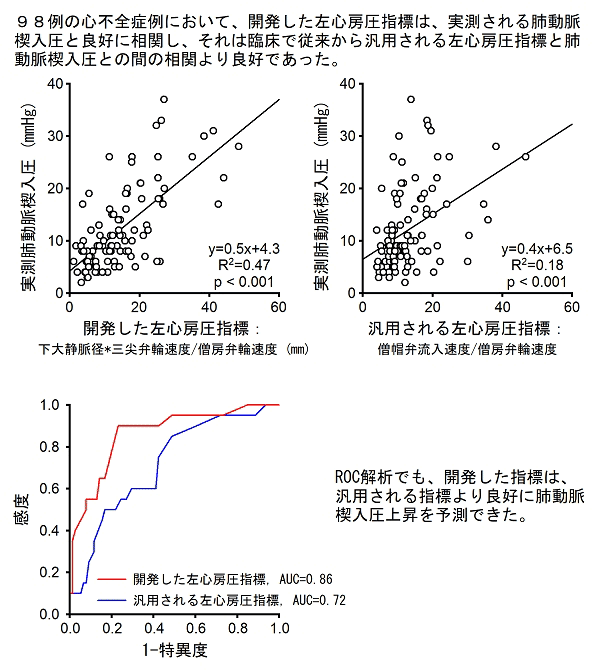
図5
関連成果等
- Uemura K, Kawada T, Sugimachi M. A Novel Minimally Occlusive Cuff Method Utilizing Ultrasound Vascular Imaging for Stress-Free Blood Pressure Measurement: A-Proof-of-Concept Study. IEEE Trans Biomed Eng. 66: 934-945, 2019.
- Uemura K, Kawada T, Inagaki M, Sugimachi M. A minimally invasive monitoring system of cardiac output using aortic flow velocity and peripheral arterial pressure profile. Anesth Analg. 116: 1006-1017, 2013.
- Uemura K, Inagaki M, Zheng C, Li M, Kawada T, Sugimachi M. A novel technique to predict pulmonary capillary wedge pressure utilizing central venous pressure and tissue Doppler tricuspid/mitral annular velocities. Heart Vessels. 30: 516-526, 2015.
- Chinen D, Nagai T, Uemura K, Aikawa Y, Motokawa T, Asaumi Y, Ogo T, Kanzaki H, Noguchi T, Anzai T, Shimizu W, Ogawa H, Sugimachi M, Yasuda S. Clinical Usefulness of an Echo-Doppler Model in Predicting Elevated Pulmonary Capillary Wedge Pressure in Patients With Heart Failure. Am J Cardiol. 123: 1464-1469, 2019.
- Uemura K, Kawada T, Zheng C, Sugimachi M. Less Invasive and Inotrope-Reduction Approach to Automated Closed-Loop Control of Hemodynamics in Decompensated Heart Failure. IEEE Trans Biomed Eng. 63: 1699-708, 2016.
- 血管弾性指標値測定装置、血圧測定装置及び血管弾性指標値測定方法 特許出願 2016-009129 (2016/01/20)
- 左心房圧計測装置の作動方法および左心房圧計測装置 特許登録 2013-024296(2013/02/12)
最終更新日:2021年10月01日
