バイオデジタルツイン研究部
1. バイオデジタルツインとは?
デジタルツインとは、現実空間にある情報をデータ分析・処理を経て、仮想空間に環境を再現する仕組みです。モデル上でシミュレーションを行い、予測やモノづくりに生かす試みは幅広い分野で行われています。医療においても脳や心臓の病気を高精度にモデル化し、患者一人ひとりの治療効果を高める取り組みが全世界で行われており、デジタルツインを用いたアルツハイマー病の治療の臨床試験も始まっています(日本経済新聞: https://www.nikkei.com/article/DGXZQOUF2773T0X21C22A0000000/)。
心血管系は物理的動作が主要な機能であることから、数理的モデルへの展開が、他臓器に比べて容易であるという特徴があります。国循とNTT-Rの共同研究チームは、心臓を中心とした循環のモデルを単純な電気回路モデルを基礎として構築し、患者個々の循環モデルを仮想空間に再現できることを目指しています。これができることで、生体情報のインプットさえあれば、その患者の何が問題なのか?を瞬時に把握できるだけでなく、さまざまな治療シミュレーションが可能になることから、患者個々の病態や状況に合わせた最適化や将来的には自動治療(医師不要・医師以上の最適個別化治療の提供)も考えることができます。また、無数の心血管モデルを生成することで、仮想空間のみで臨床研究を行うような未来もあり得ると考えています。

自動治療システム:ACIS構想
https://vimeo.com/897450724/a410ec56fb
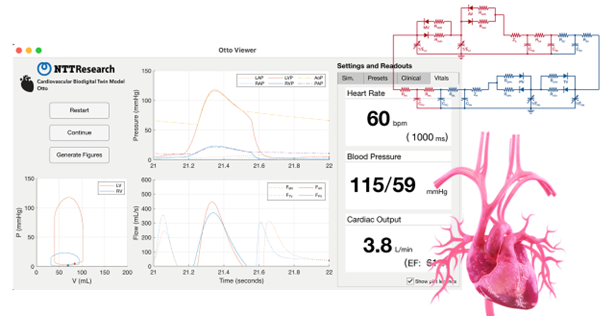
心臓・循環シミュレーターOtto:BioDT構想の基礎
https://vimeo.com/911263900/ecbc7b1435?share=copy
2. NTT Research社との共同研究
NTT Research社(本社:カリフォルニア州サニーベール)のMedical & Health Informatics Laboratories(MEI研究室)は、高精度なAIと生理学ベースの計算モデルを活用することで、さまざまな疾患の複雑さに対処するバイオデジタルツイン(BioDT)の取り組みを行っています。最初のターゲットは心血管系であり、循環の数理モデルを用いた心血管BioDTを開発しています。しかしながら、複雑な病態生理の再現のためには、このモデルに自律神経調節、適応、加齢など、心血管におけるさまざまな生理現象や応答を組み込む必要があります。
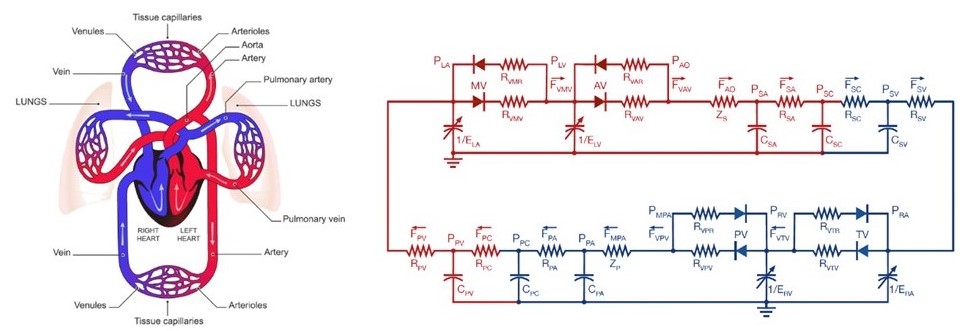
循環動態制御部は、心力学や循環平衡理論などを基礎とした自律神経調節による循環調節やストレス応答などをこれまでに研究し、数理モデル化を行っています。また、急性心筋梗塞や急性心不全、敗血症性ショックなどの状態において、薬剤投与の自動治療介入に関する先進的な技術を有しています。また、小動物〜大型動物を用いた仮説の検証や概念実証(POC)のためのウェットラボ施設を保有しています。
両者の目的は一致しており、相補的、相乗的に研究を推進できると考えられたことから、循環動態制御部とNTTRのMEI研究室は、2020年より2年半にわたるモデリング・シミュレーションおよび動物実験による検証に重点を置いた共同研究を行ってきました(https://www.ncvc.go.jp/topics/20210209/)。研究が進み、これらの技術の臨床応用に向けたさらなる拡大が必要と考えられたことから、循環動態制御部とMEI研究室は国循にバイオデジタルツイン研究部を設立することになりました。
・臨床応用をゴールとした、専門的かつ多様な研究チームの形成
・動物実験や臨床試験による開発物の検証
・学際的な共同研究の枠組みによる若手研究者の育成
・医学研究、医療技術イノベーションの推進
を本部門では進めていきます。
3. バイオデジタルツインを応用した自動治療システムの開発
医師は急性心不全などの重症循環不全症例に相対する時に、自分の経験・自分の頭の中で構築する血行動態のイメージ・ガイドラインなどに基づいて治療方法の選択や調整を行います。また、多くの治療において機械(シリンジポンプ、ECMOコンソールなど)を制御しています。しかし、頭の中のイメージは、モヤっとしていて、定量性に欠け、時間空間的な一貫性に欠けます。つまり、明確なモデル化まではされていない状態です。
BioDTとは、対象とする生身:Bioの人間(患者あるいは健常人)の心臓血管の状態と、双子:Twinのようにそっくりな心臓血管モデルが、デジタル:Digitalでつまりコンピュータ上で再現されたものです。よって、その現実との相似性、相同性は非常に重要となりますし、それは、目的に応じて適切な解像度である必要があります。本研究部では、BioDTのさらなる開発のために、心臓血管システムを平衡状態という視点からモデル化する循環平衡理論や動的視点からもモデル化できるプラットフォームのさらなる先進化、肺循環などの特異的な血管システムのモデル化に取り組んでいます。さらに、生体に備わった自律的な心臓血管制御系である自律神経システムの制御メカニズムの解明も推進しています。また、心臓血管作動薬等の薬物治療や、コロナ治療でも使われたECMO等の機械的循環補助装置による治療の効果を、コンピュータ上の双子で再現する試みを行っています。
モデルが確立すると制御に研究を進めることができます。我々は、BioDTに基づいた急性心不全や敗血症性ショックの循環制御システムを開発し、動物実験による検証結果を報告してきました。BioDTによって、定量化された循環動態の把握が可能となるだけでなく、治療の自動化・自律化が可能であることを見出し、その潜在的有用性と有効性をひしひしと実感してきました。この自動治療システムを臨床現場で安心して使えるように、日夜研究開発に邁進しています。もちろん、BioDTモデルや治療システムの臨床応用のためには、生身の人間・循環器疾患患者の実データに基づいたモデル・システム開発が必要となるため、国立循環器病研究センターの臨床部門との共同研究にも着手しつつあります。
本邦のみならず全世界的な(少なくとも先進国における)高齢化の進展により、急性心筋梗塞や心不全のような循環器疾患患者は、現在そしてこれからも爆発的に増加していきます。一方で、このような方々をケアできる人的・物的なリソースは先細りしていくことは容易に想像できます。このような状況を打破するうえで、循環器疾患治療の治療を自動化・自律化するシステムの開発に大きな社会的意義があり、未来があることは疑う余地がありません。
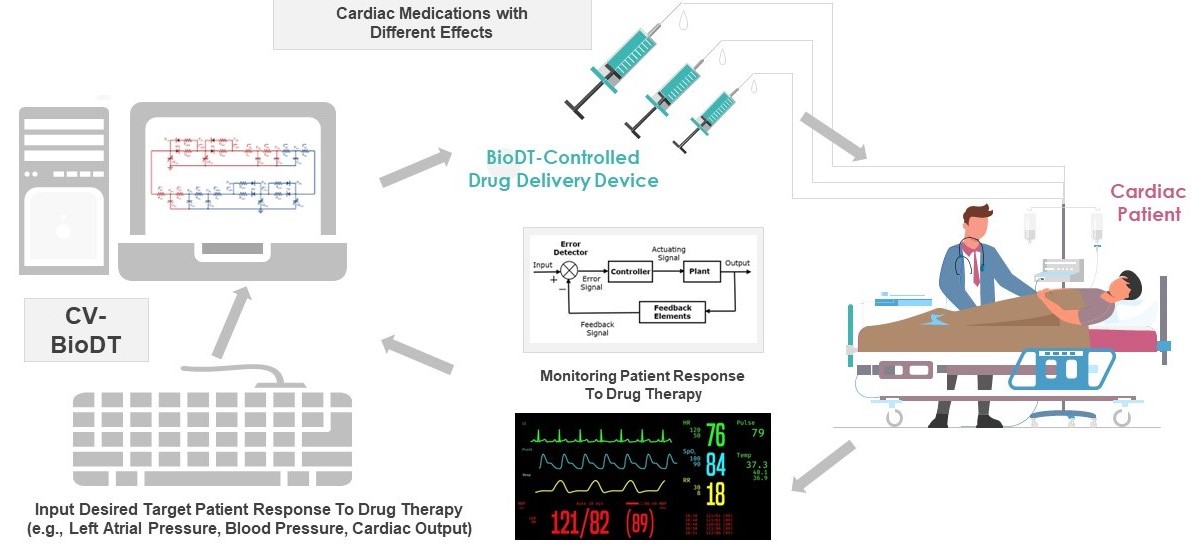
4. メンバー募集
バイオデジタルツイン研究部は、医学のみならず、工学や情報学、生理学などを融合した極めてユニークな研究や開発を推進しています。非常に重要な観点は、生体の記述を行い、適切なモデル化を目指すということです。これは、全ての医療職種・生物系研究者に役立つ経験だと考えています。若手の研究者・医療従事者の方で興味をお持ちになりましたら、ぜひとも当部スタッフのメールアドレスにご連絡ください。
5. 参考文献
循環平衡、PV loopに関する研究
- Left ventricular interaction with arterial load studied in isolated canine ventricle. Am J Physiol. 1983, 245(5 Pt 1):H773-80.
doi: 10.1152/ajpheart.1983.245.5.H773. - A novel framework of circulatory equilibrium. Am J Physiol Heart Circ Physiol. 2004, 286(6):H2376-85.
doi: 10.1152/ajpheart.00654.2003. - Prediction of circulatory equilibrium in response to changes in stressed blood volume. Am J Physiol Heart Circ Physiol. 2005, 289(1):H301-7.
doi: 10.1152/ajpheart.01237.2004. - Prediction of the impact of venoarterial extracorporeal membrane oxygenation on hemodynamics. Am J Physiol Heart Circ Physiol. 2015, 308(8):H921-30.
doi: 10.1152/ajpheart.00603.2014. - Prediction of hemodynamics under left ventricular assist device. Am J Physiol Heart Circ Physiol. 2017, 312(1):H80-H88.
doi: 10.1152/ajpheart.00617.2016. - Total Mechanical Unloading Minimizes Metabolic Demand of Left Ventricle and Dramatically Reduces Infarct Size in Myocardial Infarction. PLoS One. 2016, 28;11(4):e0152911.
doi: 10.1371/journal.pone.0152911. - Mechano-chronotropic Unloading During the Acute Phase of Myocardial Infarction Markedly Reduces Infarct Size via the Suppression of Myocardial Oxygen Consumption. J Cardiovasc Transl Res. 2019, 12(2):124-134.
doi: 10.1007/s12265-018-9809-x. - The Partial Support of the Left Ventricular Assist Device Shifts the Systemic Cardiac Output Curve Upward in Proportion to the Effective Left Ventricular Ejection Fraction in Pressure-Volume Loop. Front Cardiovasc Med. 2020, 7:163.
doi: 10.3389/fcvm.2020.00163. eCollection 2020. - Prediction of haemodynamics after interatrial shunt for heart failure using the generalized circulatory equilibrium. ESC Heart Fail. 2020, 7(5):3075-3085.
doi: 10.1002/ehf2.12935. - Prediction of hemodynamics after atrial septal defect closure using a framework of circulatory equilibrium in dogs. Am J Physiol Heart Circ Physiol. 2020, 319(5):H938-H947.
doi: 10.1152/ajpheart.00098.2020.
自律神経調節に関する研究
- Open-loop static and dynamic characteristics of the arterial baroreflex system in rabbits and rats. J Physiol Sci. 2016, 66(1):15-41.
doi: 10.1007/s12576-015-0412-5. - Systematic understanding of acute effects of intravenous guanfacine on rat carotid sinus baroreflex-mediated sympathetic arterial pressure regulation. Life Sci. 2016, 149:72-8.
doi: 10.1016/j.lfs.2016.02.051. - Closed-Loop Identification of Baroreflex Properties in the Frequency Domain. Front Neurosci. 2021, 15:694512.
doi: 10.3389/fnins.2021.694512. - Quantitative assessment of the central versus peripheral effect of intravenous clonidine using baroreflex equilibrium diagrams. J Physiol Sci. 2021, 71(1):39.
doi: 10.1186/s12576-021-00824-y. - Angiotensin II inhibition increases diuresis during acute sympathetic activation in intact and denervated kidneys in rats with chronic myocardial infarction. Heart Vessels. 2022, 37(9):1636-1646.
doi: 10.1007/s00380-022-02110-2. - Early donepezil monotherapy or combination with metoprolol significantly prevents subsequent chronic heart failure in rats with reperfused myocardial infarction. J Physiol Sci. 2022, 72(1):12.
doi: 10.1186/s12576-022-00836-2. - Linear and nonlinear identification of the carotid sinus baroreflex in the very low-frequency range. Physiol Rep. 2022, 10(14):e15392.
doi: 10.14814/phy2.15392. - Impact of neurally mediated antidiuretic effect relative to pressure diuresis during acute changes in sympathetic nerve activity. Am J Physiol Regul Integr Comp Physiol. 2023, 324(1):R82-R89.
doi: 10.1152/ajpregu.00205.2022. - Dynamic accentuated antagonism of heart rate control during different levels of vagal nerve stimulation intensity in rats. Am J Physiol Regul Integr Comp Physiol. 2023, 324(2):R260-R270.
doi: 10.1152/ajpregu.00229.2022. - Acute effects of empagliflozin on open-loop baroreflex function and urine glucose excretion in Goto-Kakizaki diabetic rats. J Physiol Sci. 2023, 73(1):7.
doi: 10.1186/s12576-023-00861-9.
自動治療に関する研究
- Automated drug delivery system to control systemic arterial pressure, cardiac output, and left heart filling pressure in acute decompensated heart failure. J Appl Physiol 2006, 100(4):1278-86.
doi: 10.1152/japplphysiol.01206.2005. Epub 2005 Dec 22. - Adaptive predictive control of arterial blood pressure based on a neural network during acute hypotension. Ann Biomed Eng. 2004, 32(10):1365-83.
doi: 10.1114/b:abme.0000042225.19806.34. - Comprehensive physiological cardiovascular model enables automatic correction of hemodynamics in patients with acute life-threatening heart failure. Conf Proc IEEE Eng Med Biol Soc. 2006, 198-201.
doi: 10.1109/IEMBS.2006.259935. - Computationally managed bradycardia improved cardiac energetics while restoring normal hemodynamics in heart failure. Ann Biomed Eng. 2009, 37(1):82-93.
doi: 10.1007/s10439-008-9595-8. - Automated drug delivery system for the management of hemodynamics and cardiac energetic in acute heart failure. Annu Int Conf IEEE Eng Med Biol Soc. 2010, 5222-5.
doi: 10.1109/IEMBS.2010.5626279. - Automated Cardiovascular Drug Infusion System to Control Hemodynamics. Adv Biomed Eng. 2013, 2: pp. 32-37.
doi.org/10.14326/abe.2.32 - Less Invasive and Inotrope-Reduction Approach to Automated Closed-Loop Control of Hemodynamics in Decompensated Heart Failure. IEEE Trans Biomed Eng. 2016, 63(8):1699-708.
doi: 10.1109/TBME.2015.2499782. - Computer-controlled closed-loop drug infusion system for automated hemodynamic resuscitation in endotoxin-induced shock. BMC Anesthesiol. 2017, 17(1):145.
doi: 10.1186/s12871-017-0437-9. - Low-Dose Landiolol Reduces Heart Rate and Cardiac Oxygen Consumption Without Compromising Initial Hemodynamic Resuscitation in a Canine Model of Endotoxin Shock. Shock. 2019, 52(1):102-110.
doi: 10.1097/SHK.0000000000001224. - Development of an automated closed-loop β-blocker delivery system to stably reduce myocardial oxygen consumption without inducing circulatory collapse in a canine heart failure model: a proof of concept study. J Clin Monit Comput. 2022, 36(3):849-860.
doi: 10.1007/s10877-021-00717-w.
最終更新日:2024年02月13日
