細胞生物学部
概要
循環器は、心臓と脈管(血管・リンパ管)からなります。心臓は、心筋脂肪・血管構成細胞・線維芽細胞が緻密な発生制御過程により組み合わされて構成されます。血管は内皮細胞・血管平滑筋細胞で構成され、内腔に血液を通すために透過性調節が可能な特殊な構造も持ち合わせています。この循環システムが受精・発生・成熟過程でどのように出来上がっていくかを生体イメージングと分子細胞生物学的に同時解析することで、形態形成とその制御過程を理解する研究を行っています。
哺乳類は母体内で発生しますので、成長を時間経過で観察することは、容易ではありませんが、ゼブラフィッシュ胚を用いると3日間くらいで循環システム(心臓・脈管)が構築されますので全経過を可視化することが可能です。
心臓も血管構築細胞もいずれも両側の中胚葉から発生して、心臓と血管が結合することで心臓―動脈―臓器・組織―静脈―心臓という閉鎖循環系が成立します。この閉鎖循環系を成立するためには、逆流や効率のよい臓器への酸素・栄養源の供給が可能となる複雑な構造をとることが要求されます。この詳細な構造の形成過程を調節する情報伝達系の解析をイメージングにより行っています。
これまで発生学的なアプローチにより研究を進めて参りましたが高齢化社会に不可避である加齢による循環臓器の組織学的変化・機能低下についても調べていくことで治療法の開発に結び付けたいと思います。
研究テーマ
- 血管形成機構の解明
- 心臓発生機構
2-1 一次心臓領域と二次心臓領域形成の調節シグナル
2-2 心内膜による冠血管形成誘導機構 - 肺胞形成(血管内皮細胞による調節)
- pH 感受性細胞応答機構
1.
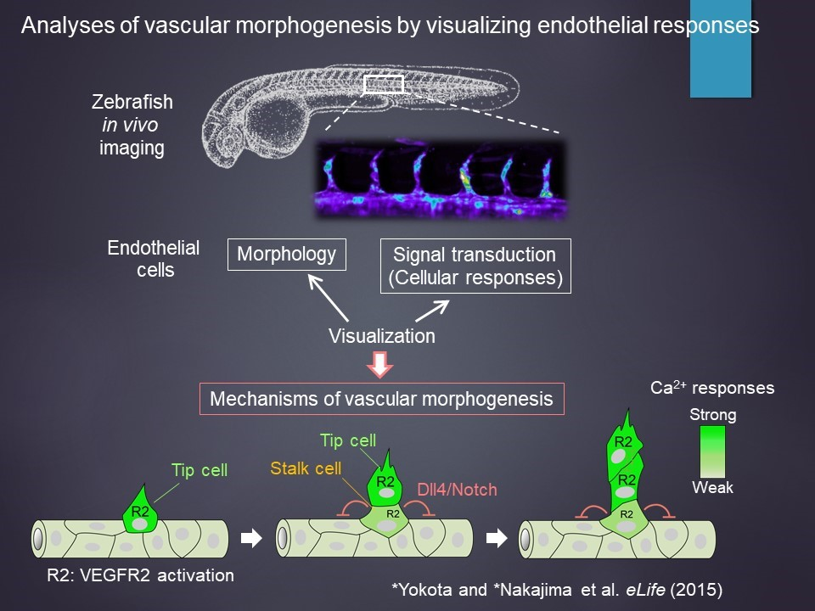
血管ネットワークを構築するためには、血管内皮細胞が外部環境(分泌因子や力学的刺激など)に応答することが必要である。我々は、ゼブラフィッシュを用いた蛍光生体イメージングによって、細胞の形態と細胞内シグナル伝達と同時に可視化することで血管形成過程を捉えている。血管内皮増殖因子VEGFA/VEGFR2シグナルの活性化を、その下流で応答する細胞内カルシウムのイメージングによって、生きたまま間接的に捉えることに成功している(eLife, 2015)。
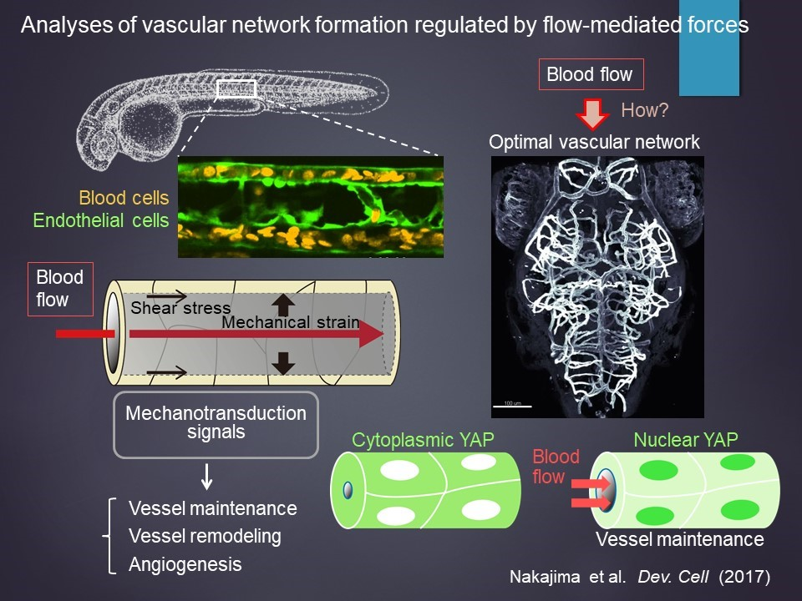
血流は、酸素や栄養などの運搬のみならず、流れ自体が細胞にメカノトランスダクションを誘発することで血管の維持やリモデリング、血管新生に重要な役割を果たすことが知られている。血管構造・血管応答・血流を同時可視化して、血流に対する新たな細胞応答を捉えることに成功している。Hippo経路の標的因子であるYAPが血流に応答して活性化し、血管の恒常性維持に寄与することを明らかにした(Developmental Cell, 2017)。
2-1.
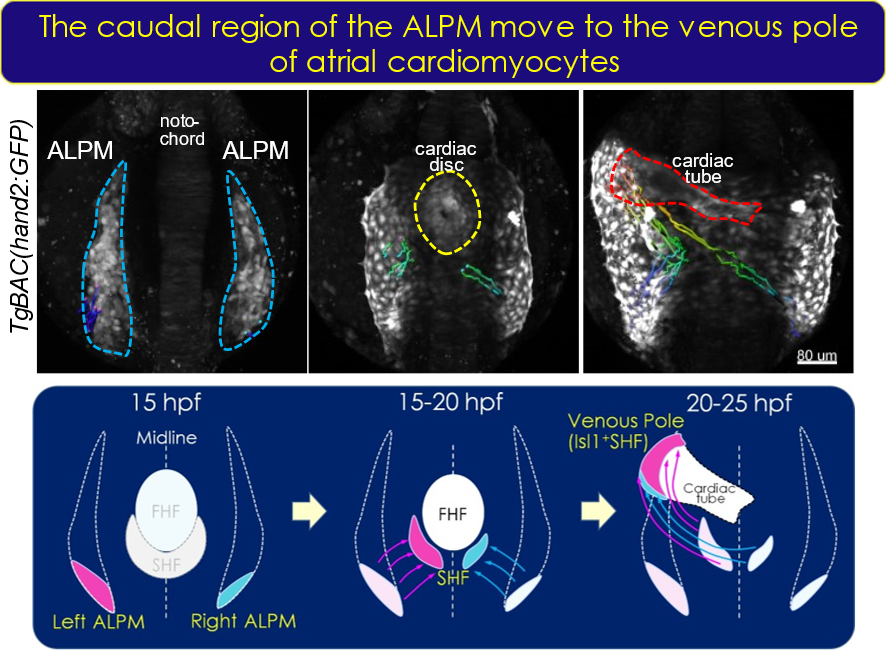
心筋細胞は一次心臓領域(FHF)と二次心臓領域(SHF)に由来する細胞から発生してくる。ゼブラフィッシュのSHFはIslet1 (Isl1) を発現する細胞から成り、流入路と流出路を構成する。我々は心臓発生過程を解析してきたなかで、心房流入路近傍でHippoシグナルのエフェクター:Yap/Wwtr1が活性化することを見出した。Bmp2bがHippoシグナルの下流で発現制御され、心筋の前駆細胞である前方側板中胚葉(ALPM)からの分化段階にHippoシグナル-Bmp/Smadシグナルが作用することを見出した。さらに弁形成機構における血流の重要性も検討中である。
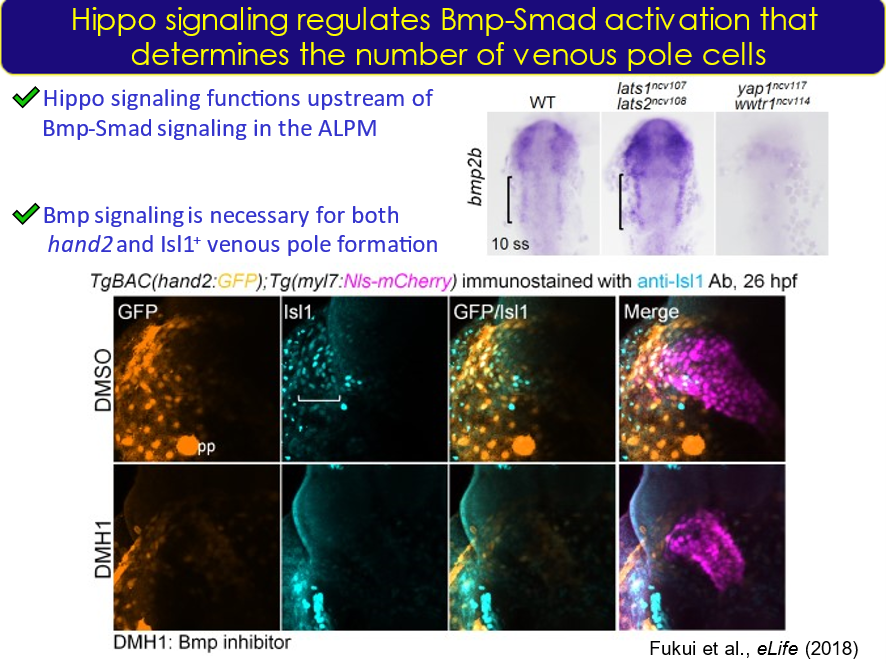
2-2.
心筋も多様な心筋細胞から構成されている。ゼブラフィッシュ心は、一心房一単心室であり、哺乳類よりも単純な構造をしているが、様々な形態の心筋細胞から構成されている。部位ごとに、異なる機能を有した心筋細胞が存在することをシグナル可視化モニターリングフィッシュでつきとめた。Wnt シグナル活性化細胞が冠血管形成に必須であることを検討中である。
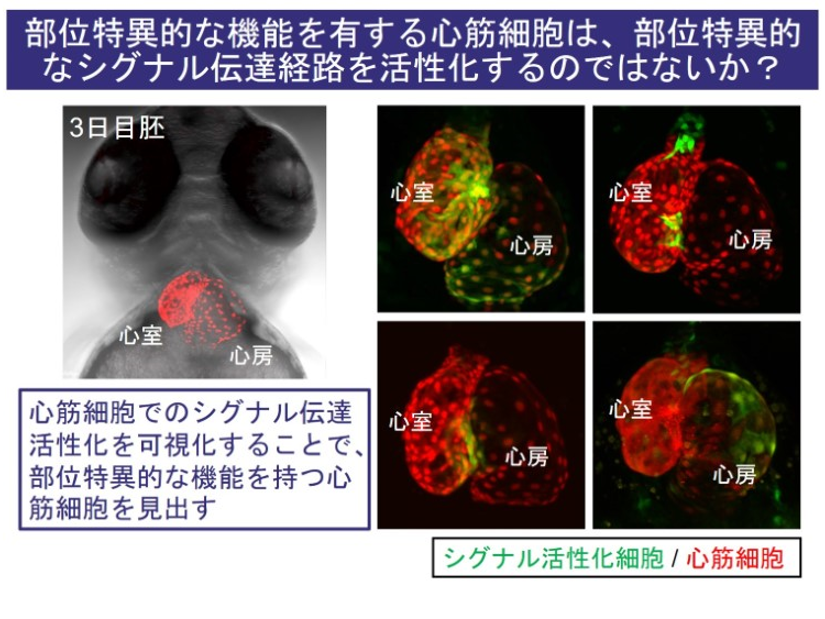
3.
マウスの出生直後の肺は、気管支末端の終末嚢から構成される「肺胞」は存在しない。しかし、生後3日から肺胞筋線維芽細胞が急激に出現し、終末嚢に隔壁を作ることによって多数の「肺胞」が形成される (図A)。この急速で劇的な肺胞形成過程では、platelet-derived growth factor receptor alpha (PDGFRa陽性の線維芽細胞が、II型肺胞上皮細胞が分泌するPDGF-A依存的に平滑筋aアクチン(a-smooth muscle actin, a-SMA)陽性の肺胞筋線維芽細胞へと分化し、強い収縮力を発揮して終末嚢を分割する(図A)。同時に血管内皮細胞がこの肺胞形成に如何にかかわるかを検討している。
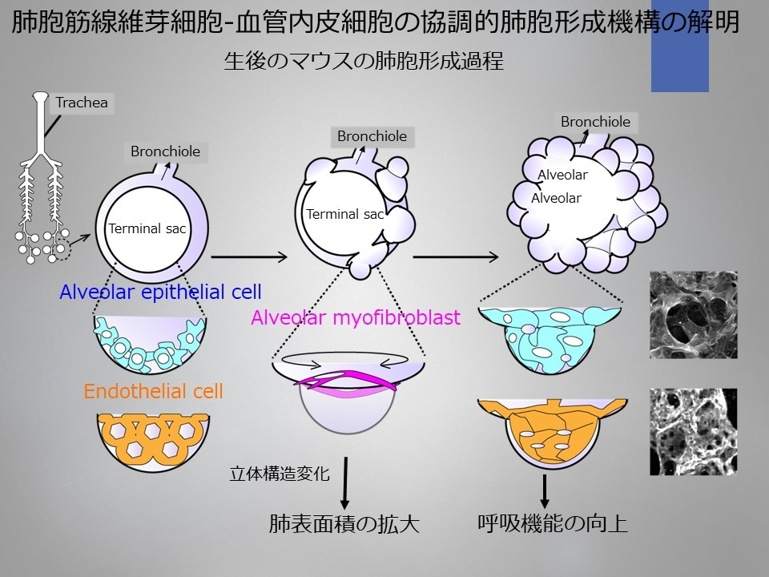
4.
体内の細胞外酸性度(以下pH)は、細胞内の酵素やチャネル分子として機能するタンパク質の活性を至適に保つために、通常pH7.4付近に保たれている。細胞から排出されたプロトンや炭酸ガスは、血液を通して肺と腎臓に運ばれ、体外に排出されて全身性にpHが維持される。一方で、局所的には、生理的な条件下でも血中pHは増減していると予想できる。しかし、局所で起きる血中pHの変化に対し、血液に直接晒される血管内皮細胞(以下内皮細胞)が、pHに応じた生理機能調節を行なっているかどうか、殆ど明らかにされていない。そこで内皮細胞のpH応答性を突き止めて、生体内で常に変動するpH条件下でどのように内皮細胞が機能しているのかを解明し、内皮細胞の新たな調節機構を理解したい。我々は、細胞内外のpH変動をモニターできるプローブを全身性に発現するゼブラフィッシュ系統の樹立に成功した。今後、血管内皮細胞特異的なプロモータ下でプローブを発現させたゼブラフィッシュ個体や、培養細胞系を用いてpH変動と内皮細胞応答機能の関係を明らかにする予定である。
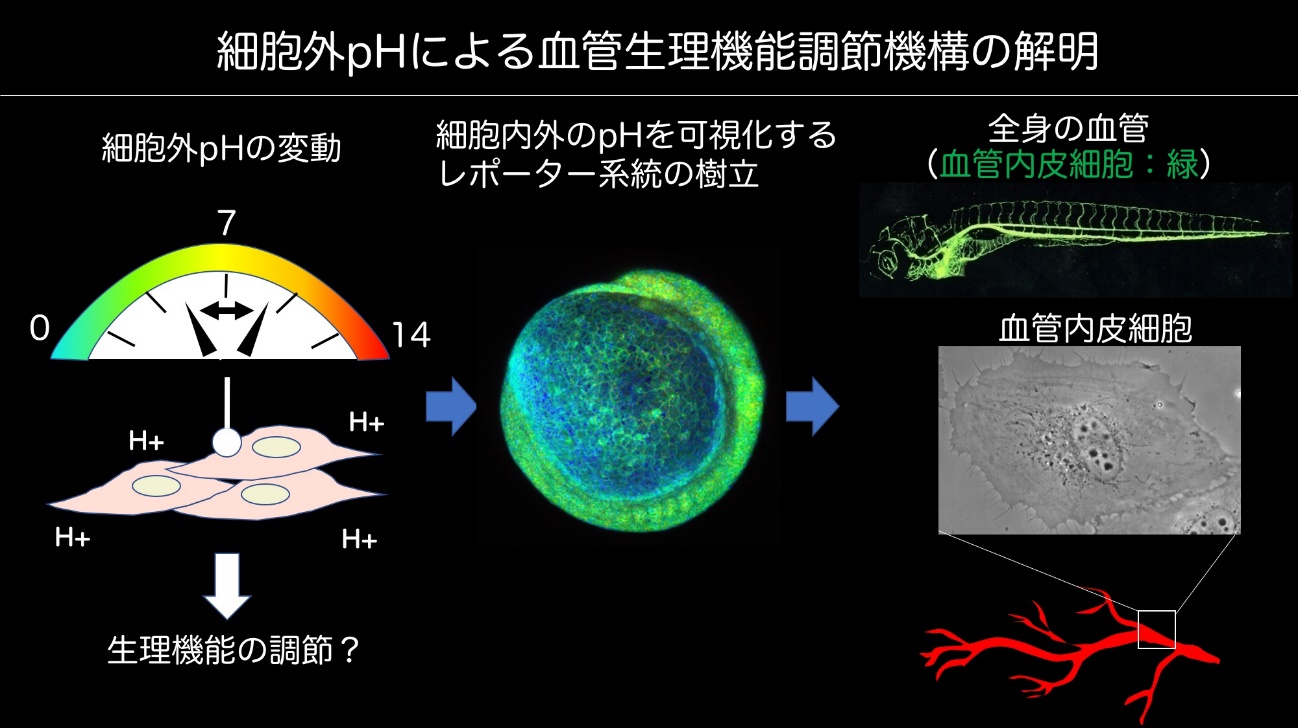
最終更新日:2021年10月05日
