広報活動
心筋自己再生を誘導する新規遺伝子Klf1の発見
令和3年4月9日
国立循環器病研究センター
国立循環器病研究センター (大阪府吹田市、理事長:大津 欣也、略称:国循)研究所・再生医療部の小川 真仁 上級研究員、菊地 和 部長らとビクター・チャン心臓病研究所 (豪州)の研究チームは、ゼブラフィッシュ(注1)を用いて成熟心筋細胞の再生誘導で中心的に機能する転写因子Krüppel-like factor 1 (Klf1) の同定に成功しました。本研究成果は、アメリカ科学振興協会の学術雑誌「Science」に令和 3年 4月 9日付で掲載されました。
背景
高い再生能を持つゼブラフィッシュの心臓が損傷されると、成熟心筋細胞はその収縮構造を減らし、一時的に幼弱化する脱分化(注2)と呼ばれる状態を経て増殖し、失われた心筋を自己再生することができます。近年、再生能を持たないと考えられてきたマウス、ラット、ブタなどの哺乳類も、生後数日の間はゼブラフィッシュと同様に心臓を自己再生することが分かってきました。自己再生を標的とする新たな心筋再生療法の確立が期待されていますが、その基盤となる心筋細胞の脱分化・増殖誘導機序の理解は不十分でした。
研究手法と成果
心筋細胞の脱分化・増殖を制御する新規分子の同定を目指し、まず再生中のゼブラフィッシュの心臓で発現が上昇する遺伝子を網羅的に探索し、得られたデータを転写因子に着目して解析しました。転写因子はDNAに結合し、遺伝子発現を調節するタンパク質の一群であり、細胞の成熟度や機能の変化に関わることが少なくありません。その結果、再生心臓で発現が上昇する転写因子としてKlf1が同定されました。Klf1は赤血球の分化に必須な転写因子であり、致死性の先天性貧血の原因遺伝子としてよく知られていますが、心臓での機能は全く未知でした。
まず、心臓を損傷したのち時間経過を追ってKlf1の発現変化を調べたところ、損傷後に誘導されたKlf1発現は心筋細胞増殖の増加と相関して上昇し、再生終了時に沈静化することが分かりました。さらに、心筋組織切片を用いてKlf1遺伝子がどの細胞で発現するか解析したところ、心筋細胞特異的に発現することが示され、その心筋機能が示唆されました。そこでゲノム編集技術を用いて心筋特異的にKlf1の発現を抑制するゼブラフィッシュ系統を作製したところ、Klf1欠損心筋細胞は脱分化、増殖反応を減じ、再生不全を呈することが明らかとなりました(図1A)。これらの結果は、よく知られた赤血球機能とは異なり、Klf1は心筋細胞の自己再生を制御するという全く新規の機能を持つことを示していました。
心筋再生におけるKlf1の重要性を探るため、人為的なKlf1発現により損傷のない心臓においても強制的に心筋再生が誘導され得るか検証しました。その結果、わずか7日間の心筋特異的なKlf1発現により、広範な心筋細胞に脱分化、増殖の亢進が見られ、1ヶ月後の心臓が顕著に肥大し(図1B)、心筋細胞数は約5倍に増加しました(図1C)。したがって、Klf1は単独で心筋細胞の自己再生を誘導する強力な再生機能を有します。
次に、このKlf1の顕著な再生誘導機能を理解するため、Klf1を発現した心臓を用いて遺伝子発現やクロマチン構造の変化を網羅的に解析しました。その結果、Klf1は心筋細胞のクロマチン構造を変化させ、心筋分化の遺伝子ネットワークを特異的に抑制することで脱分化を誘導することが分かりました。また、細胞増殖に関わる様々な遺伝子の発現を上昇させることも分かりました。さらに代謝変化の網羅的解析を行った結果、Klf1の発現によりミトコンドリアを介する通常のエネルギー代謝が低下し、代わりにDNA合成やアミノ酸などの新しい細胞を作る上で必須な構成成分の産生経路が上昇することが分かりました。以上の結果から、Klf1は遺伝子発現調節、クロマチン構造変化、および代謝経路の再配列を適切に制御し、心筋自己再生プログラムの誘導において「スイッチ」のように働く極めて重要な転写因子であると考えられます(図1D)。
今後の展望と課題
本論文ではゼブラフィッシュの心臓におけるKlf1の顕著な心筋自己再生誘導能を報告しました。Klf1を中心とする「心筋再生スイッチ」がヒトなどの哺乳類の心筋細胞においてどの程度保存されるか、またそのスイッチに介入することで再生プログラムを誘導できるか否か、などは今後の重要な研究課題と言えます。Klf1の研究がさらに進み、将来今回報告した研究成果を基盤とする新たな心筋再生療法の確立が実現することを期待します。
注1:ゼブラフィッシュの稚魚は透明で体の構造を見るのに適している。また、成魚に成長したのちも心臓や中枢神経などを再生することができる。脊椎動物であることからヒトと体の構造や発生において多くの共通点があり、発生・再生研究の良いモデル生物となっている。
注2:未分化マーカーの発現、サルコメアなどの筋収縮構造の減少が心筋細胞の脱分化を示す特徴として知られる。
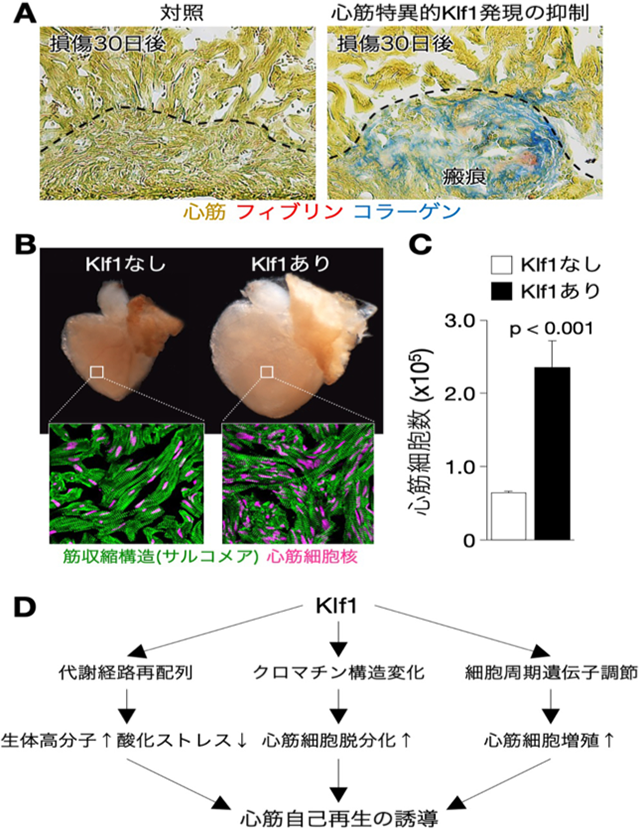
図1.
(A) 心筋特異的Klf1発現の抑制による心筋再生不全。
(B) 非損傷心臓におけるKlf1の心筋自己再生亢進。
(C) Bの心臓における心筋細胞数の計測。
(D) 心筋自己再生におけるKlf1機能 (詳細は論文に記載)。
発表論文情報
著者:Masahito Ogawa, Fan-Suo Geng, David T. Humphreys, Esther Kristianto, Delicia Z. Sheng, Subhra P. Hui, Yuxi Zhang, Kotaro Sugimoto, Maki Nakayama, Dawei Zheng, Daniel Hesselson, Mark P. Hodson, Ozren Bogdanovic, and Kazu Kikuchi
題名:Krüppel-like factor 1 is a core cardiomyogenic trigger in zebrafish
掲載誌:Science
謝辞
本研究は、下記機関より資金的支援を受け実施されました。
・日本学術振興会 科研費(助成金番号:JP20H03683)
・National Health and Medical Research Council(NHMRC)(助成金番号:1160466)
・Australian Research Council(ARC)(助成金番号:DP190103852)
最終更新日 2021年04月09日
最終更新日:2021年09月26日
