広報活動
心不全につながる難病「肺高血圧症」の重症化メカニズムを解明~既存治療薬に抵抗性の重症肺高血圧症に新しい治療の可能性~
令和3年3月9日
国立循環器病研究センター
日本医療研究開発機構
国立循環器病研究センター(大阪府吹田市、理事長:小川久雄、略称:国循)血管生理学部の中岡良和部長らの研究グループが、肺動脈性肺高血圧症の発症・重症化において、芳香族炭化水素受容体の活性化が重要な役割を果たしていることを明らかにしました。
本研究の成果は、米国科学アカデミー紀要(Proceedings of the National Academy of Sciences of the United States of America)に3月8日15時(米国時間EST)にオンライン掲載されました。
背景
肺動脈性肺高血圧症(Pulmonary arterial hypertention: PAH*1)は肺高血圧症のひとつで、心臓から肺に血液を送る肺動脈に狭窄や閉塞が生じて肺動脈圧が上昇する疾患であり、最終的には心不全(右心不全)へ進行する予後不良の難治性疾患です。これまでPAHの発症には遺伝的な因子だけでなく、環境因子や炎症の関与も重要であると考えられてきました。しかしながら、環境因子がどのような形でPAHの発症・重症化にかかわっているのかは不明でした(1)。
一般に環境ホルモン受容体として知られる芳香族炭化水素受容体(AHR)は、生体外から取り込まれる化学物質の解毒に関わる酵素を発現誘導したり、炎症性シグナルをコントロールすることから、AHRとPAH発症・重症化との関係を検討することにしました。
研究手法と成果
PAH患者と健常者のボランティアより得られた血液がAHRをどの程度活性化させるのか検討したところ、PAH患者の血液の方がAHRを強く活性化し、AHRの活性化能が高い患者ほど重症で予後が不良であることが明らかとなりました(図1)。また、ラットに、代表的なAHR活性化物質6-formylindolo[3,2-b]carbazole(FICZ)を投与すると重症PAH患者と同様の血管病変を伴う、重症のPAHが誘導されました(図2上)。そこで、AHRを欠損させたラットを作製し、既存の方法で重症PAHを誘導しましたが、PAHは起こりませんでした(図2下)。つまり、重症PAHの原因がAHRであることが明らかになりました。また、近年注目されている薬剤誘発性PAHの一つである青黛*2誘発性PAHの原因であることも明らかにしました。さらに、網羅的な遺伝子発現解析などから、血管内皮細胞と骨髄由来細胞のAHRの活性化が炎症性シグナルを活性化させることでPAHを誘導していることがわかりました(図3)。以上の結果から、血液が有するAHR活性化能の測定が、PAHの予後を予測するバイオマーカーとなり、AHRやその関連分子に対する阻害剤が重症PAHの治療薬として有望であることが示唆されました。
今後の展望と課題
現在、PAHに対しては、エンドセリン受容体拮抗薬、ホスホジエステラーゼ5(PDE5)阻害薬、プロスタサイクリン受容体作動薬などが使用されておりますが、これらの薬剤を使用しても病気の進行を抑制できない症例が存在し、治療応答性の低い症例の予後は依然として不良であることが知られています。本研究で得られた成果は、こうした症例の早期発見と、治療薬や病気の進行の予防薬の開発につながる可能性を示しています。
<引用文献>
- M. Humbert et al., Pathology and pathobiology of pulmonary hypertension: state of the art and research perspectives. The European respiratory journal 53 (2019).
<注釈>
*1)肺動脈性肺高血圧症(PAH)
心臓から肺に血液を送る血管を肺動脈と呼び、その肺動脈の血圧が異常に上昇する疾患を総称して肺高血圧症と呼びます。肺動脈性肺高血圧症は、特に、肺動脈の異常に起因するものを指します。この病気では、肺の細い動脈が異常に狭くなるために、血液の流れが悪くなり、狭い血管を無理に血液が流れるように心臓が努力することで、肺動脈圧が上昇します。適切な治療がなされないと、最終的に心不全(右心不全)から死に至ります。発症原因は完全には分かっておらず、厚生労働省の指定難病の1つです。
*2)青黛
青黛は漢方として使用され、染料のインディゴなどを含有し、潰瘍性大腸炎の治療にしばしば使用されます。近年、青黛を服用した潰瘍性大腸炎の患者にPAHが発症するケースが日本で報告されており注目されています。本研究では、青黛誘発性PAHの原因がAHRであることを同定しました。
発表論文情報
著者: Takeshi Masaki, Makoto Okazawa, Ryotaro Asano, Tadakatsu Inagaki, Tomohiko Ishibashi, Akiko Yamagishi, Yasushi Sakata(大阪大学大学院医学系研究科循環器内科学), Takeshi Ogo, Tadamitsu Kishimoto(大阪大学免疫学フロンティア研究センター), Yoshikazu Nakaoka et.al.
題名: Aryl hydrocarbon receptor is essential for the pathogenesis of pulmonary arterial hypertension
掲載誌: Proceedings of the National Academy of Sciences of the United States of America
DOI: 10.1073/pnas.2023899118
謝辞
本研究は、下記機関より資金的支援を受け実施されました。
文部科学省科学研究費 (H16-05298, H20-03682, H20-08484)
国立研究開発法人日本医療研究開発機構(AMED) 難治性疾患実用化研究事業
「メタボローム情報に基づく肺―腸―腸内細菌相関による肺動脈性肺高血圧症の発症機構」
国立研究開発法人国立循環器病研究センター循環器病研究開発費(30-2-3)
公益財団法人ヤクルト・バイオサイエンス研究財団、公益財団法人武田科学振興財団、
公益財団法人第一三共生命科学研究振興財団、公益財団法人喫煙科学研究財団、岸本基金
<図表>
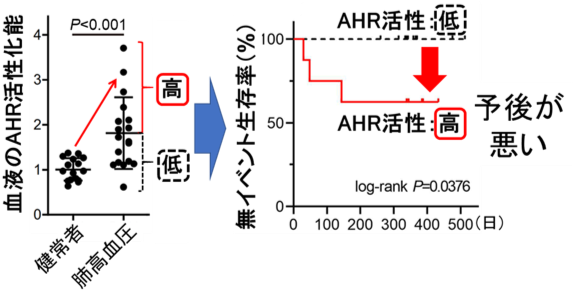
図1.肺高血圧症患者では、血液のAHRの活性化能が上昇しており、活性化能が高いほど重症で予後不良である。 (健常者16名、肺高血圧18名、肺高血圧AHR活性高値群8名、低値群10名、バーは標準偏差を示す。)
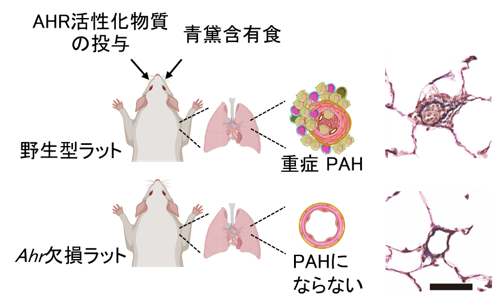
図2.野生型ラットではFICZ等のAHR活性化物質を投与すると内膜病変を伴う重症PAHを誘発した。しかし、AHR欠損ラットでは、PAHが誘発されなかった。
AHR活性化物質を含む青黛の投与でもPAHが誘発されたが、AHRを欠損させると、同様にPAHが誘発されなかった。
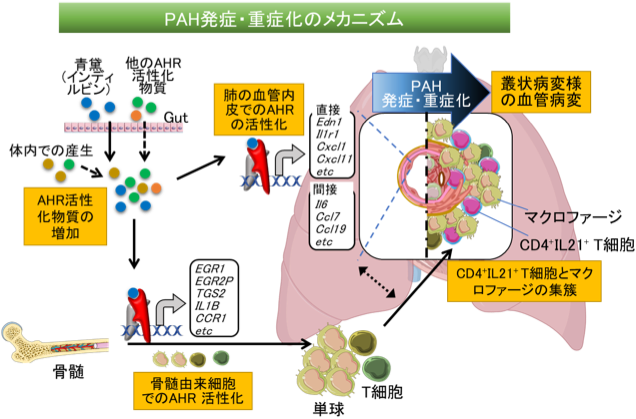
図3.腸から吸収される食物や薬物、その他体内で生成した物質などにより、肺や骨髄由来の血液細胞のAHRが活性化され、肺局所での炎症や、骨髄由来のCD4陽性IL-21陽性T細胞やマクロファージが肺へ集まってくる。その結果肺血管に変化が起こり、肺高血圧症となる。
最終更新日 2021年03月09日
最終更新日:2021年09月26日
