広報活動
脳梗塞の新しい動物モデル(マウス)を確立 ~脳梗塞の新たな治療法開発に寄与すると期待~
国立循環器病研究センター(略称:国循)猪原匡史脳神経内科医長、再生医療部の服部頼都流動研究員らの研究チームは、国循 画像診断医学部の飯田秀博部長、圓見純一郎研究員らの研究チームと共同で、脳梗塞の治療薬の開発に利する新規の脳梗塞の動物モデルの創出に成功しました。本研究成果は、米国神経科学会誌「Journal of Neuroscience」に3月4日(日本時間)付で掲載されます。
■研究のポイント
・新しい脳梗塞の動物モデルをマウスで確立した。
・これまで困難であった白質(神経線維の束)に脳梗塞を再現できた。
・脳梗塞の新規治療法の開発に役立つ動物モデルと期待される。
■研究の背景
脳梗塞を主体とする脳血管疾患は我が国の死因の第4位、寝たきりの第1位の原因であり、新規治療法の開発が急がれていますが、国民医療費総額の実に1割近くが脳卒中診療に費やされているにも関わらず、決め手となる治療法がないのが現状です。「夢の薬」と謳われているアルテプラーゼ(tPA, tissue plasminogen activator)ですら,発症から4.5時間以内に投与を受けられる患者さんはわずか数%であり,新たな治療法の開発が望まれています。しかし、海外で行われた脳梗塞に対する大規模臨床試験は脳保護薬などを含めtPA以外すべて失敗に終わっており、その原因の一つとしてこれまでの治験薬がマウス等げっ歯類の灰白質(神経細胞の塊)に脳梗塞を起こすモデルを用いて評価・開発を行ってきたが、ヒトの脳梗塞の場合は、心臓由来の血栓による脳梗塞(心原性脳梗塞)を除けば灰白質よりも白質(内包や放射冠などと呼ばれる神経線維の束)の部分が障害されて運動麻痺や感覚障害を起こすことがむしろ多いということが挙げられます。
そこで、今回猪原医長らの研究チームは白質選択的に脳梗塞を起こすマウスの確立を目指しました。
■研究手法と成果
現在、脳循環不全を誘導するマウスのモデルとして2004年に開発された両側総頸動脈狭窄モデル(通称,BCASモデル)が国内外で広く使われており、猪原医長がその確立に関わりました(Shibata M, et al. Stroke 2004)。このBCASモデルは両側の総頸動脈に微小なコイルを装着することで作成され、白質が粗になる粗鬆化は見られますが脳梗塞までは起こらないため、ヒトで多くみられる白質の梗塞を対象とした治療薬の評価には用いることが出来ませんでした。しかし今回開発した「左側狭窄,右側緩徐閉塞モデル」(asymmetric common carotid artery surgeryモデル;ACASモデル)では、左側の総頸動脈を微小コイルで狭窄させ右側の総頸動脈をアメロイドコンストリクターと呼ばれる緩徐に動脈を狭窄させ最終的に閉塞させるデバイスを用いて、脳の循環をゆっくりと低下させ白質に脳梗塞を誘導することに初めて成功しました。(図1~3)
■今後の展望と課題
脳梗塞の治療法の研究開発が遅滞してきた一つの理由として、脳の白質部位選択的に脳梗塞を再現できるげっ歯類のモデルがなかったことが挙げられます。しかし今回白質選択的に脳梗塞を再現できるマウスモデルを確立したことから、今後は本モデルを用いて新規脳梗塞治療薬の開発-応用のサイクルを循環させることが可能となると考えられます。既存のBCASモデルは脳循環不全のモデル動物として最も優れていると現在のところ評価されていますが、本研究で開発したACASモデルはBCASモデルの弱点を克服したモデルとして今後広く用いられていくことが期待できます。
■掲載紙と公表日時
Hattori Y, Enmi J, Kitamura A, Yamamoto Y, Saito S, Takahashi S, Iguchi S, Tsuji M, Yamahara K, Nagatsuka K, Iida H, Ihara M. A novel mouse model of subcortical infarcts with dementia. J Neurosci, in press 米国神経科学会誌:米国・東部時間2015年3月3日17時(日本時間3月4日(火)7時)
■本研究は、下記機関より資金的支援を受け実施されました
・文部科学省「基盤研究(B)」(猪原)
・文部科学省「萌芽研究」(服部)
・文部科学省「基盤研究(C)」(圓見)
・厚生労働省「創薬基盤推進研究事業」(猪原)
・公益財団法人武田科学振興財団「ビジョナリーリサーチ」(猪原)
【図1.】 脳血流の推移(レーザースペックル法による脳表血流の解析)
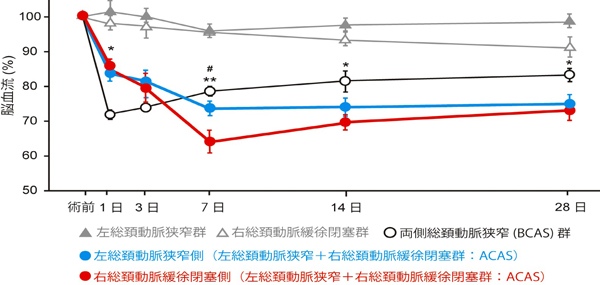
血流の推移を手術前の値を100(%)として示す.既存のBCASモデル(-○-)では,脳血流が手術前(pre),手術後1日,3日,7日,14日,28日の脳手術後1日目に前値の70%まで低下し,その後緩徐に回復していくという推移を取るが,新規のACASモデル(-●-,左微小コイル装着側;-●-,右アメロイドコンストリクター装着側)では,緩徐に脳血流が低下し,その後も脳の循環不全が維持される.ACASモデルは慢性的な脳循環不全の状態をよりよく再現できる動物モデルと言うことが出来る.なお,左側のみの狭窄群(-▲-)と右側のみの緩徐閉塞群(-△-)では,ほとんど脳血流は低下しない.
【図2.】 頭部MRI画像(7テスラMRI拡散強調画像(冠状断)による解析)
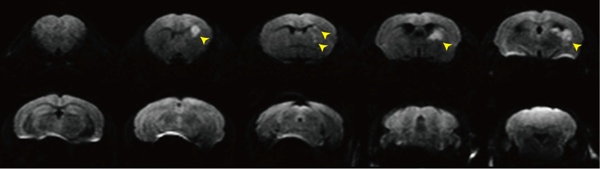
手術後8日目,脳梁を中心とした脳梗塞が誘導されている(黄矢頭).これまで汎用されてきた脳表の灰白質に脳梗塞を誘導するモデルと異なり,慢性的な脳循環不全を誘導することで,脳の深部,特に白質を中心に脳梗塞を誘導することが出来る初のモデルが確立できた.
【図3.】 ACASモデルの運動機能障害と作業記憶障害の評価
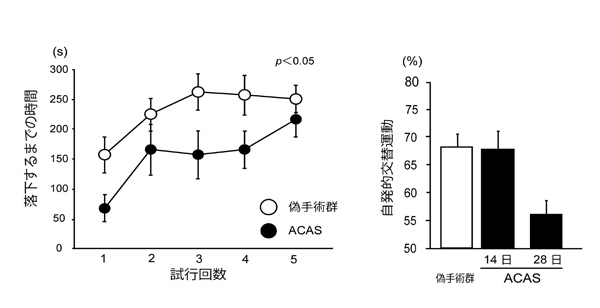
(A) ACASモデルの術後14日目のロータロッド法による運動機能評価では,ACAS群(-●-)は偽手術(コントロール)群(-○-)と比較して運動機能が劣っており,運動障害を呈していることが示される.
(B) ACASモデルの術後14日目と28日目にそれぞれ作業記憶を評価した(Y迷路試験による評価).偽手術群(コントロール群)と比べて,術後14日目には作業記憶の障害は起こらないものの,術後28日目には作業記憶障害が見られた.
最終更新日 2015年03月06日
最終更新日:2021年09月26日
