広報活動
心血管病モデルマウスの拍動心臓で冠動脈と心筋の収縮機能を高精度で観察可能とする画像解析法を開発
<循環器病の分子レベルの仕組みと治療法の開発を加速・促進する技術>
平成24年12月26日
独立行政法人国立循環器病研究センター
公益財団法人高輝度光科学研究センター
独立行政法人国立循環器病研究センター 研究所の白井幹康(心臓生理機能部長)と公益財団法人高輝度光科学研究センター(兵庫県佐用郡佐用町、理事長:白川哲久)の八木直人(利用研究促進部門副部門長)および梅谷啓二(同部門主幹研究員)らの研究チームは、大型放射光施設SPring-8の高輝度X線を用い、循環器疾患モデルに多用されているマウスやラットなどの拍動心臓において微小な冠動脈の収縮・拡張機能を観察する技術と心筋収縮を起こす蛋白質分子の運動機能を解析する技術を世界に先駆け共同開発し、循環器病の分子レベルの仕組みを解明してきました。この度、その成果が米国Circulation Research誌に高く評価され、一連の研究成果をまとめたレビューが米国の1月4日に電子版として発表されます。
開発した技術は、高速で拍動する小動物の心臓に応用できる画像解析法で、1)冠動脈の太い部分から細い部分(約30μm径)までの血管応答を心臓全体で観察可能とする放射光高分解能微小血管造影法と、2)心臓収縮の力の源となる心筋の収縮蛋白質分子の運動を心室の様々な部位においてピンポイントで評価可能とする放射光X線回折法です。これらの技術は、循環器病の遺伝子・蛋白質レベルのメカニズム解明や治療法開発の加速・促進につながるものと期待されます。
![]() 研究の背景
研究の背景
マウスなどの小動物は、遺伝子導入や欠損などの遺伝子操作技術が確立し、また、短期間での病態モデル作成が容易であることから、試験管で行われる遺伝子・蛋白質レベルの研究を個体に還元して検証する研究において重要な位置をしめています。しかし、小動物において、循環調節に直結する心筋の収縮・弛緩機能や脳、心臓、肺、腎などの血管機能を生きた個体で観察することは技術的に容易とはいえません。特に、体が小さく(20 g程度)、高心拍数(約500拍/分)のマウスでは、高速に動いている心臓での微小冠動脈の異常な収縮や閉塞などは観察困難でした。また、心臓の収縮・拡張を引き起こす心筋細胞内の蛋白質分子の運動機能障害も評価不可能でした。このような小動物生体における心血管機能の観察限界は、循環器病の分子メカニズムの解明に遺伝子改変技術や病態モデル作製技術を充分に活かせない一要因となっていました。
![]() 研究手法と成果
研究手法と成果
開発した以下の研究法は、SPring-8の高輝度放射光X線の特性を生かしたものです。
1)放射光高解像度微小血管造影法
この造影法では、血管を映し出すために血管内に注入するヨード性造影剤のX線吸収が特異的に高まる波長のX線を放射光から選択的に取り出し、さらに、高速メカニカルシャッターによってビデオ信号に同期したパルスX線(露光時間1~2 ms)にして、目的部位に照射します。このような特殊なX線で、高濃度分解能及び対象物の動きに伴う画像のブレの最小化(ストロボ画像化)を実現します。撮像カメラは1インチX線撮像管サチコンで、最小7μmの分解能で血管撮影を可能とします。
図1A, Bは、特殊X線を当てながら、麻酔下マウスの上行大動脈にヨード性造影剤を微量注入し、冠動脈造影を行ったものです。高速で拍動する心臓の冠動脈の本管(約150μm径)から細動脈(約30μm径)レベルまでの血管応答が鮮明に映し出されています。また、図Cでは、右心室から肺動脈幹、さらに肺微小動脈までが連続的に観察できます。図2では、国循の寒川研究所長が発見したアドレノメデュリン(AM)のラット虚血心臓での血管新生効果と血管内皮機能改善効果が画像で明確に示されています。
2)放射光X線回折法
上記の血管造影法は、X線が造影剤で吸収されてできる影を利用した方法ですが、本法は、X線が心筋細胞内の収縮蛋白質分子であるアクチン(A)とミオシン(M)に当たり、散乱された後、干渉し合ってできる回折像を解析する方法です。
AとMは規則正しく配列した六角格子構造を形成し、この構造内にはMだけが配列する(1,0)格子面とMとAが配列する(1,1)格子面があります(図3B)。この規則正しい構造により、散乱X線は干渉し回折像を作りますが、(1,0)格子面に由来する回折ピークを(1,0)反射、(1,1)格子面由来を(1,1)反射と呼びます(図3C)。心筋収縮時にはMの頭部がA側へ移動・結合することで力を発生しますが(図3A)、これは、Mだけの(1,0)格子面からAとMで構成される(1,1)格子面への質量移動を意味し、回折像では(1,0)反射の輝度I1,0の低下と(1,1)反射の輝度I1,1の増加として現れます。実際の解析には、輝度比I1,0/I1,1を用い、輝度比低下の度合いはM頭部のAへの移動・結合数とほぼ比例します。弛緩時は逆に輝度比は増加します。
図4は、20週齢の自然発症高血圧ラット(SHR)の肥大心臓の左心室前壁と後壁に0.2x0.2 mmの放射光マイクロビームを当て、約10心拍に渡り回折像の(1,1)反射輝度に対する(1,0)反射輝度の比の変化を記録したものです。前壁では輝度比は心拍に合わせて規則正しく増減しており、ミオシン頭部のアクチンへの正常な周期的結合・離脱が示唆されます。しかし、後壁の輝度比は心拍と同期しない不規則な変化となっており、結合・離脱機能の障害が示唆されます。このラットの心臓全体のポンプ機能には異常は見つかっていないことから、放射光マイクロビームを使った心筋X線回折法は、心臓局所の心筋収縮蛋白質機能のピンポイント評価法として極めて有効と考えられます。
![]() 今後の展望
今後の展望
1)放射光高解像度微小血管造影法
心臓、脳、肝臓、腎臓などの固形臓器の内部を走る微小血管の応答は、臓器機能に直結するにも関わらず、これまで観察できませんでした。高解像度微小血管造影法はあるがままの臓器血管ネットワークを可視化し、さらに臓器内の血流分布や循環時間も観察可能とします。循環調節関連の遺伝子を改変した種々のマウスへの応用によって、各臓器の循環調節や血管病の遺伝子・蛋白質レベルの仕組みが明らかになると期待されます。また、本法は、血管再生の評価にも応用できるので、心筋梗塞、脳梗塞などの虚血性疾患後の血管新生のメカニズム解明や、血管再生治療の評価にも応用できます。
2)放射光X線回折法
現在、心筋収縮蛋白質分子の運動を拍動する心臓から非侵襲的にリアルタイムで計測できる手法は本法以外にはありません。この方法は、心室の前、後壁などの異なる心筋局所や心外膜下層、中層、内膜下層の異なる心筋層での収縮蛋白質機能のピンポイント診断を可能にしました。今後、iPS細胞などを使った心筋再生療法の評価や、心筋の神経、液性調節分子の解析法とのカップリングによる心筋生理・病態の解明への応用が期待されます。
以上の1)と2)の方法を循環器病モデル小動物に組み合わせて応用すれば、様々な心臓・血管病の分子レベルの仕組みの解明が進み、それに基づく根本的治療法の開発が加速するものと期待されます。
![]() 補足説明
補足説明
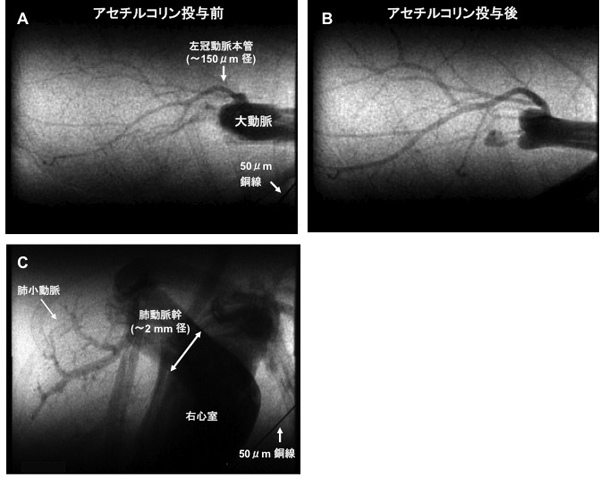 |
| 図1 麻酔下のマウス(心拍数~500拍/分)で可視化した冠動脈(A,B)と右心室から肺動脈(C) 冠動脈が本管から細動脈(~50μm径)まで、心臓全体に渡って一望できる(A)。血管内皮から血管拡張性物質を放出させるアセチルコリンを投与すると、広範囲の血管枝が拡張した(B)。右心室から肺動脈幹、さらに肺小動脈まで連続した観察もできる。 |
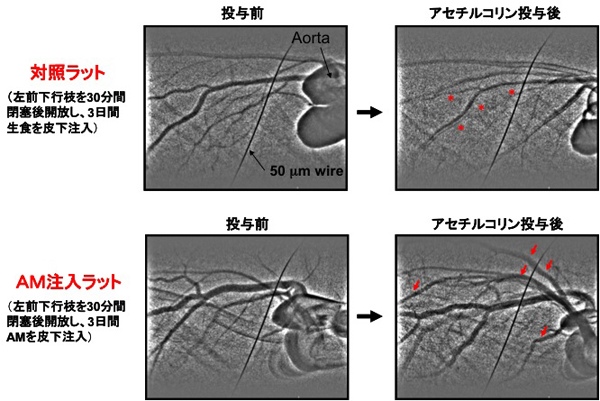 |
| 図2 アドレノメデュリン(AM)はラット心臓虚血再灌流後の冠細動脈内皮機能を改善する 麻酔下でラットの左冠動脈前下行枝を30分間閉塞して開放し、覚醒後3日間飼育した。その飼育の期間、対照ラットでは生理食塩水を、 AM注入ラットではAMを持続的に皮下注入した。その後、再度麻酔し、この微小血管造影を記録した。血管内皮から血管拡張性物質を放出させるアセチルコリンを投与すると、無治療の対照ラット(上段の2つの図)では異常な血管収縮(米印)が起こったが、AM注入ラット(下段の2つの図)では正常な拡張応答(赤矢印)が起こった。また、AM注入ラットでは、対照ラットと比べ、アセチルコリン投与前の血管数が多いことから、血管新生が促進されていることが分かる。 |
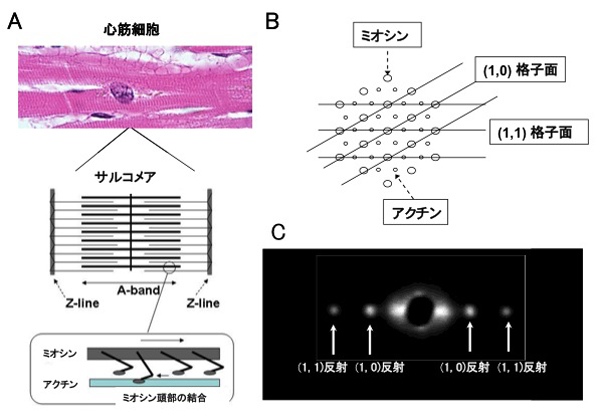 |
| 図3 心筋収縮タンパク質分子の六角格子状配列とそのX線回折像 A: 心筋細胞の横紋を拡大するとサルコメア(筋節)が見えてくる。筋節でのA帯(A-band)では、アクチンとミオシンが重なりあっている。収縮時にはミオシン頭部がアクチンへ移動・結合することにより力が発生する。 B: 筋節のA帯の横断面を示している。細いアクチンと太いミオシンが六角格子状に配列する。ミオシンだけが配列する(1,0)格子面とミオシンとアクチンが配列する(1,1)格子面が見られる。 C: 心筋X線回折像の一例。内側には(1,0)格子面を反映する(1,0)反射、外側には(1,1)格子面を反映する(1,1)反射が観察できる。心筋収縮時には、ミオシン頭部がアクチンに移動・結合するため、(1,0)格子面から(1,1)格子面に質量移動が起こる。従って、(1,1)反射の輝度は増強し、(1,0)反射の輝度は減少する。結果、(1,0)反射の輝度と(1,1)反射の輝度の比(I1,0/I1,1)は減少する。心筋弛緩時には、逆に増大する。 |
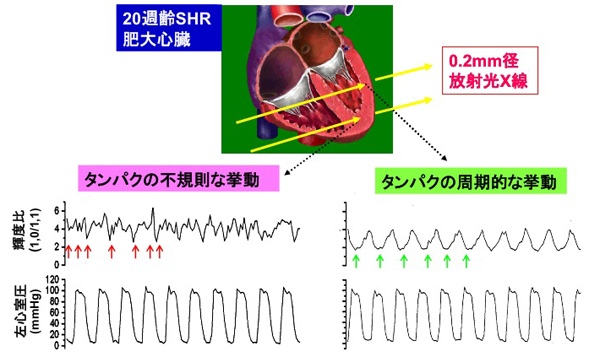 |
| 図4 自然発症高血圧ラット(SHR)の肥大心臓から10心拍に渡って記録した輝度比と左心室圧の変化 正常な心筋では、ミオシン頭部のアクチンへの結合と離脱は周期的に繰り返している。その結合と離脱を反映する輝度比は、前壁では心拍リズムに同調した正常な周期的変化(緑矢印)を示したが、後壁では異常な不規則変化(赤矢印)を示した。このことから、心筋収縮蛋白質機能の障害は、心臓全体で均一に進行するのではなく、心臓局所ごとに不均一に進行することが分かった。放射光X線回折法は収縮蛋白機能障害の不均一性進展をピンポイントで診断可能とする方法である。 |
最終更新日 2013年07月05日
最終更新日:2021年09月28日
